Для этого в 1 л воды постепенно добавляют заранее сделанные по 5 мг навески щавелевой кислоты, проверяя с помощью индикаторной бумаги показатель рН раствора. Соединяясь с кальцием и магнием, оксалат-ионы высвобождают карбонат- и сульфат-ионы. Первые присоединяют водород, разлагаются до углекислого газа и воды и практически не влияют на величину рН раствора. Вторые, будучи кислотным остатком сильной кислоты, несколько снижают численное значение рН. В разных регионах вода имеет различную степень жесткости, однако освобожденные сульфат-ионы редко когда подкисляют воду до величины менее рН6. Обычно, когда реакция среды становится ниже рН6,5 — 6 , в растворе начинают накапливаться свободные оксалат-ионы. Следует запомнить количество внесенной в 1л воды щавелевой кислоты и, несколько снизив его, повторять опыт 2 — 3 раза до тех пор, пока величина рН не установится на 6 — 6,5.
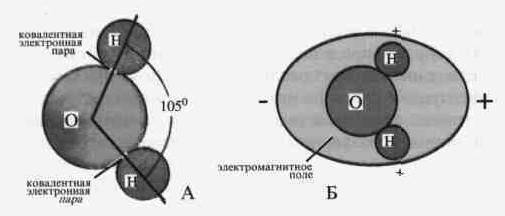
Рис. 60. Схема строения молекулы воды (А) и образование эллиптического магнитного поля вокруг атомов водорода и кислорода (Б).
Рис. 61. Схема строения макромолекулы воды, а — частично свободный отрицательный полюс и зона активности (полностью свободные полюса диполя очень быстро вступают в водородные связи и на активность воды не влияют).
После этого рассчитывают среднюю дозу щавелевой кислоты, необходимую для осаждения из воды кальция и магния.
Если же хотят сохранить кальций и магний в растворенном виде, а эти соли, например, наиболее желательны для сильно опушенных видов, то воду подкисляют азотной, соляной либо лимонной кислотой.
Большинство кактусов поглощают серу в очень незначительных количествах, поэтому во избежание закисления субстрата сульфат-ионами не следует производить корректировку реакции среды серной кислотой.
Для подщелачивания воды можно использовать состав, приведенный в предыдущей главе или же традиционно — гашеную известь, мел. Так как большинство карбонатов слаборастворимы, их следует «настаивать» и в поливную воду добавлять некоторое количество «настоя», а не осадка.
Здесь стоит пояснить, почему автор ратует за внесение щелочного компонента с водой, а не в смеси с субстратом. Только потому, что в последнем случае неизвестно, сколько растение усвоило солей кальция в процессе роста, а сколько связалось в почве в нерастворимые комплексы (при избытке эти комплексы откладываются на корневой шейке и посуде). В случае же внесения кальция в растворенном виде есть возможность его дозирования и контроля.
Еще раз напомню — показатель реакции «кислой» воды для полива кактусов лежит в пределах рН5,5 — 6,0 , «щелочной» рН7,6 — 8,0.
Говоря о воде, зная ее химическую формулу Н2О, мы представляем себе это вещество, как набор одинаковых молекул. Однако это не совсем так.
Вступая в химическую связь с кислородом, два атома водорода объединяют по одному своему электрону с электронами кислорода*. В молекуле воды атомы водорода находятся на расстоянии 105 друг от друга. Кислород же несколько задерживает общие электронные пары, в результате чего приобретает некоторый отрицательный заряд, а атомы водорода — некоторый положительный заряд. Молекула воды превращается в своеобразный магнит с отрицательным полюсом со стороны кислорода и положительным — со стороны атомов водорода, причем положительный полюс может делиться на две части. По количеству полюсов молекула воды называется диполем.
Диполи химически чистой воды соединены между собой водородными связями в одну макромолекулу, что дает возможность с некоторой долей абстракции сказать: вода в стакане — это одна макромолекула, и вода в океане — это тоже одна макромолекула.
Жидкости не имеют кристаллической решетки. Овальные диполи воды соединяются как по физическим, так и по геометрическим (пространственным) законам, ввиду чего не все положительные полюса соединяются с отрицательными. Более того, из-за особенности пространственного строения диполя, один из атомов водорода может оставаться несвязанным — образуя частично свободный положительный полюс. Если же с отрицательным атомом кислорода одного диполя способен связаться лишь один атом водорода другого — формируется частично заряженный отрицательный полюс. Вокруг таких полюсов образуются зоны активности, способные вступать в физико-химические связи с ионами и целыми молекулами.
При растворении какого-либо вещества некоторые водородные связи рвутся и диполи воды окружают свободные ионы, выстраиваясь в сложные пространственные фигуры, несколько снижая подвижность иона. В результате создается комплекс ион-диполи. Для того, чтобы разбить подобные комплексы и макромолекулы воды на отдельные молекулы, высвободить ионы, необходимые для питания, растению приходится затрачивать определенные химические вещества,
Это так называемая ковалентная связь, при которой, в отличие от ионной связи, внешние электроны не отдаются, а объединяются в общие электронные пары.
Рис. 62. Схема простейшей установки для создания
«живой воды».
В результате эллектролитической диссоциации ионы ОН" концентрируются у положительного анода, а ионы Н проходят через стенку мешка и у отрицательного катода соединяются в молекулу водорода и покидают раствор.
а, значит, и некоторую энергию.
Если же в воде порваны водородные связи и повышается количество свободных диполей или их полюсов, то такая вода становится биологически активной. Крошечные диполи воды очень подвижны, имеют огромную проникающую сквозь клеточные стенки способность и, присоединяясь к ионам, стимулируют их поступление в клетку.
В природе биологически-активная вода образуется при таянии снега, при выпадении росы, тумана или дождя. В домашних условиях биологически-активную воду можно получить, пропуская через воду постоянный ток, пропуская воду через магнитное поле, быстро нагревая воду, а затем быстро охлаждая ее, используя талую воду, предварительно заморозив ее в холодильнике. Степень эффективности такой воды прежде всего зависит от количества порванных водородных связей. Естественно, что применять активную воду следует сразу же после ее приготовления, т.к. уже через полчаса при комнатной температуре количество свободных диполей сокращается вдвое.
Хочется отдельно остановиться на так называемой «живой воде»*, т.е. на воде, у которой порваны не только водородные связи, но и частично связи между водородом и гидроксильной группой — отщеплен один из атомов водорода.
Прежде всего, как наиболее просто получить «живую воду»?
Для этого надо сшить мешок из плотного брезента или сделать стакан из отрезка пожарного рукава (в лучшем случае, используют полупроницаемые мембраны). Стакан или мешок помещают в стеклянную банку (ни в коем случае нельзя использовать металлические емкости). К двум угольным стержням присоединяют провода и один из них опускают в банку, а другой — в стакан или мешок. Всю систему заполняют водой так, чтобы вода из банки не заливалась через верхний край в стакан или мешочек, а проникала туда через стенки. Маркировка электродов зависит от того, какую воду хотят получить (она будет в банке). Когда требуется положительно заряженная вода, богатая катионами (такой водой стимулируют семена при замачивании), электрод в банке подключают к отрицательному полюсу источника постоянного тока. Если же необходима отрицательно заряженная вода, богатая анионами (ее используют в подавляющем большинстве случаев: проращивание семян, стимулирование роста корней, активация пробуждения апикальной меристемы и т.д.), то электрод в банке подключают к положительному полюсу.