Открыта природа температуры
Изучение температуры тел тесно связано с познанием природы теплоты вообще. Еще в эпоху античности мыслители-натурфилософы задавались вопросом о том, что есть тепло и нагретость. Эти ученые выдвигали самые разнообразные умозрительные гипотезы, зачастую совершенно невероятные. Только в позднем средневековье утвердилось представление о температуре как о степени нагретости тела. Подобные представления привели к изобретению термометра, а он позволил приоткрыть завесу тайны, связанной с другими загадками температуры и теплоты.
Новые открытия позволили усовершенствовать конструкцию термометра и разработать калориметрические приборы. Множество открытий принес XVII в., за время которого был совершен скачок в науке о теплоте. Выдающийся английский философ и ученый Ф. Бэкон, а вслед за ним и основатель картезианства, французский мыслитель и математик P. Декарт придерживались весьма своеобразного представления о теплоте и температуре. В то время эти понятия частично смешивались, поскольку оба феномена были взаимосвязаны и представляли собой две стороны одного явления.
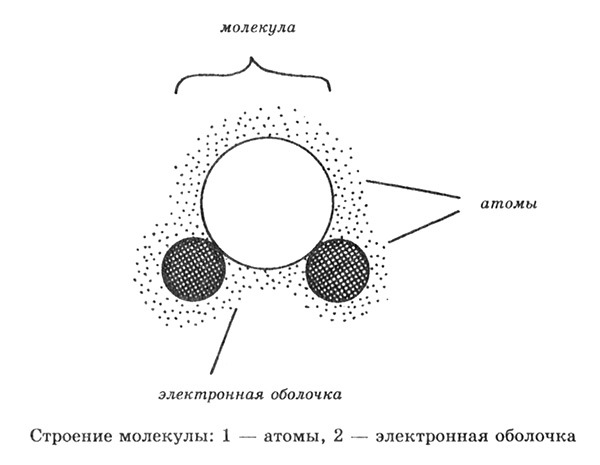
Тем не менее гипотеза Бэкона и Декарта была близка к истине. Они связали нагретость и тепло с незримым движением частиц — атомов и корпускул, из которых состоят физические тела. Но многие в то время придерживались галилеевской теории теплорода, которая восторжествовала в науке в XVIII столетии. Согласно этой теории, которая была неверной, теплота представляет собой как бы невесомую жидкость, перетекающую от одних тел к другим, сообщая им некоторую температуру.
Гипотетическую невесомую жидкость, которая в действительности не существовала, окрестили теплородом. Против теории теплорода выступали выдающиеся отечественные ученые того времени, в первую очередь М. В. Ломоносов и Г. Рихман, которые первыми начали проводить калориметрические исследования. Рихман в 1744 г. вывел формулу для вычисления степени нагретости смеси любого количества масс воды, имеющих неодинаковые температуры. Основываясь на этой формуле, шотландец Дж. Блэк обнаружил «скрытую теплоту льда», иными словами, теплоту плавления льда.
Ломоносов, сотрудничая с Рихманом, сформулировал основные положения молекулярно-кинетической теории. Он первым начал отличать атомы от молекул, внеся порядок в учение о теплоте. Несмотря на старания прогрессивных ученых, теория теплорода просуществовала в физике необычайно долго. Лишь промышленный переворот в XVIII–XIX вв. положил конец безраздельному господству ложной теории: она не могла реально объяснить преобразования теплоты в работу и наоборот, а именно эти процессы находились в центре внимания инженеров — создателей паровых машин.
К кинетическому учению вновь вернулись, оно стало непрерывно совершенствоваться. Физики догадались, что степень нагретости означает выражение внутренней энергии тела, заключающейся в хаотическом движении молекул. Такое беспорядочное движение частиц получило название теплового, но нередко его именуют броуновским по имени английского ботаника P. Броуна, который мог наблюдать под микроскопом последствия движения молекул воды. Хотя броуновское движение и имеет одинаковую природу с тепловым, в действительности оно есть следствие теплового.
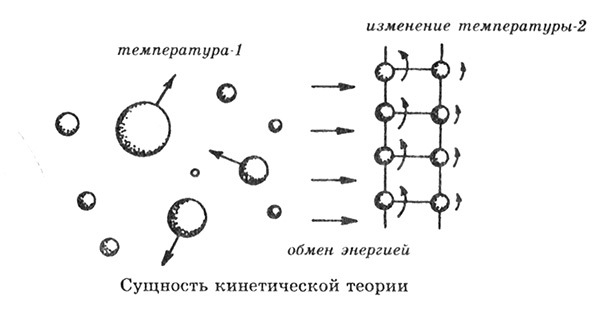
Хаотическое тепловое движение характерно для всех объектов, включая твердые тела. Степень свободы у частиц твердого тела невелика, оттого их тепловое движение представляет собой ритмичные колебания вокруг одной точки. При нагреве внутренняя энергия тела меняется, его частицы начинают двигаться быстрее. В конечном итоге прежние связи разрушаются, таким образом твердое тело переходит в жидкость с повышением температуры. В жидкости велики силы сцепления, но они допускают большую подвижность молекул. С этой особенностью связано присущее жидкостям свойство текучести.
Броун, разумеется, не мог наблюдать перемещений молекул, а лишь видел при помощи микроскопа смещения ничтожно малых растительных спор в воде. Подвижные водные молекулы ударяли по спорам растений. Суммарный удар большого числа молекул с одной стороны заставлял каждую спору двигаться в противоположную сторону, куда ударов приходилось меньше. Точно таким же образом молекулы соударяются одна с другой. Во время подобных соударений происходит обмен энергией. Всякому случалось опускать в горячий чай холодную ложечку, чтобы она его остудила.
Данный пример демонстрирует одно из неизбежных последствий молекулярного теплообмена. Быстрые молекулы горячей воды ударяют в ложечку и расшатывают ее молекулы. Энергия водных частиц растрачивается, и чай действительно немного остывает, а вот ложечка при этом обычно сильно нагревается. Получается, что горячее то тело, молекулы которого имеют наибольшую скорость (максимальную энергию). Но это касается однородных тел. Воду можно перевести в газообразное состояние, если нагреть ее до температуры +100 °C, при которой человек получает ожоги.
Однако водяной пар является газом, как и воздух, состоящий из смеси газообразных азота и кислорода. Тем не менее температура воздуха сравнительно низка, она не поднимается выше +56 °C. Дело в том, что молекулярное строение воздушных газов отлично от воды. Связи между их частицами непрочны и разрушаются уже при отрицательных температурах. Поэтому кислород становится газом при -182,96 °C, а азот — при -195,8 °C. В целом воздух как сложная смесь кипит при температуре -193 °C (все величины даны для нормального давления).
Частицы в газах обладают максимальными скоростями в мире молекул, однако разные газы получаются при разных температурах. Кипение каждого вещества происходит, если сообщить телу некоторое количество энергии. Обычно говорят о теплоте кипения. Точно так же существует теплота плавления, обнаруженная Блэком. Здесь-то как раз и проявляется разница между температурой и теплотой. Чтобы нагреть тело до определенной температуры, требуется сообщить ему некоторое количество энергии, т. е. какое-то количество теплоты.
Однако для перевода тела в новое агрегатное состояние (твердого — в жидкость, жидкости — в пар) недостаточно нагрева до температуры плавления или кипения. Нужно сообщить еще некоторое количество теплоты (энергии), которое пойдет на разрыв связей между молекулами. Вода кипит при температуре +100 °C. Однако легко представить, как надолго затянется попытка полностью перевести воду в пар посредством кипения.
Чтобы вода выкипела, мало сообщить ей температуру кипения. Требуется придать жидкости количество теплоты, необходимое для выкипания — превращения всего объема воды в пар. Оттого, к слову, ожоги от пара гораздо болезненнее, чем ожоги от кипятка. Пар обладает большим запасом энергии, т. е. большим количеством теплоты.
Кому-то может показаться, что энергия теплота тождественны. Отчасти так оно и есть. Теплота представляет собой т. н. тепловую энергию, особую разновидность энергии вообще. Этот вид энергии можно перевести в другие виды. На этом принципе основано строение всех тепловых машин: выделяемая ими теплота преобразуется в механическую энергию, которая становится работой.
Воздух насыщен водяным паром. Как же получается, что человек не обжигается этим паром. Причин тому несколько, и открыты они были учеными не сразу. Следует сказать, что молекулы пара затрачивают свою энергию вследствие соударений с «холодными» воздушными молекулами. В результате скорость движения водяных частиц в атмосфере резко падает, пар остывает. Оттого в высших ее слоях протекают процессы конденсации, осаждения капельной влаги. Вода возвращается в жидкое состояние. Из бесчисленных мельчайших капелек складываются облака.
Второй причиной является то, что мы не ощущаем ударов отдельных молекул, а газы в атмосфере сильно перемешаны. Поэтому конденсация влаги протекает лишь на больших высотах, где падение температуры воздуха более чем заметно. Смешение молекул с разными скоростями приводит к тому, что средняя скорость частицы воздуха резко отличается от максимально и минимально возможных значений. Получается, что воздух состоит из усредненных молекул, определяющих его температуру, которую можно ощущать и измерить.