Важное место в К. занимает физика реального кристалла, изучающая различного рода дефекты в кристаллах (центры окраски, вакансии, дислокации, дефекты упаковки, границы кристаллических блоков,доменов, зёрен и т. д.) и их влияние на физические свойства кристаллов. Такими свойствами, в первую очередь, являются пластичность, прочность, электросопротивление, люминесценция, механическая добротность и т. д. К задачам К. относится также поиск новых кристаллов, обладающих физическими свойствами, необходимыми для практических применений.
Лит. см. при ст. Кристаллография,Кристаллы, Симметрия кристаллов.
К. С. Александров.
Кристаллофосфоры
Кристаллофосфо'ры (от кристаллы и греч. phōs — свет, phóros — несущий), неорганические кристаллические люминофоры. К. люминесцируют под действием света, потока электронов, проникающей радиации, электрического тока и т. д. Способность К. люминесцировать обусловлена наличием запрещенной зоны в энергетическом спектре кристалла (см. Твёрдое тело), поэтому К. могут быть только полупроводники и диэлектрики. В состав К. входят в малых концентрациях примеси — активаторы. Активаторы и дефекты решётки кристалла (вакансии, междуузельные атомы и т. п.) образуют центры свечения. Механизм свечения К. в основном рекомбинационный (см. Люминесценция). Люминесцировать К. могут как в результате возбуждения непосредственно центров свечения, так и при поглощении энергии возбуждения кристаллической решёткой К. и передаче её (через электроны и дырки, экситоны и др.) центрам свечения. Непосредственная рекомбинация электронов и дырок в К. также сопровождается свечением (излучательная рекомбинация). Длительность послесвечения К. колеблется в широких пределах — от 10-9сек до нескольких часов. В зависимости от активатора спектр люминесценции К. может меняться от ультрафиолетового до инфракрасного.
Основой К. служат сульфиды, селениды и теллуриды Zn, Cd, оксиды Ca, Mn, щелочно-галоидные и некоторые др. соединения. В качестве активаторов используют ионы металлов (Cu, Со, Mn, Ag, Eu, Tu и т. д.). Синтез К. осуществляется чаще всего прокаливанием твёрдой шихты, однако ряд К. получают из газовой фазы или расплава. Комбинируя активаторы и основы, можно синтезировать К. для преобразования различных видов энергии в видимый свет необходимых цветов с высоким кпд (до десятков %). Созданы, например, К., преобразующие инфракрасное излучение в видимое, а также К., яркость люминесценции которых возрастает или уменьшается (вспышечные и тушащиеся К.) под действием инфракрасного излучения. Благодаря таким широким возможностям, а также большой яркости свечения, химической и радиационной стойкости К. находят значительное применение (особенно К. с шириной запрещенной зоны в несколько эв). Порошкообразные К. используются в люминесцентных лампах, экранах телевизоров и осциллографов, электролюминесцентных панелях и т. д. К. с малым временем послесвечения (например, NaI·Tl) применяются в сцинтиляционных счётчиках для регистрации быстрых элементарных частиц и g-квантов. Некоторые К. могут выступать в качестве активной среды в полупроводниковых лазерах.
Лит.: Фок М. В., Введение в кинетику люминесценции кристаллофосфоров. М., 1964; Физика и химия соединений AII, BVI, пер. с англ., М., 1970.
Э. А. Свириденков.
Кристаллохимия
Кристаллохи'мия, изучает пространственное расположение и химическую связь атомов в кристаллах, а также зависимость физических и химических свойств кристаллических веществ от их строения. Будучи разделом химии, К. тесно связана с кристаллографией. Источником экспериментальных данных о кристаллических структурах являются главным образом рентгеноструктурный анализ, структурная электронография и нейтронография, с помощью которых определяют абсолютные величины межатомных расстояний и углы между линиями химических связей (валентные углы). К. располагает обширным материалом о кристаллических структурах нескольких тысяч химических веществ, включая такие сложные объекты, как белки и вирусы.
Основные задачи К.: систематика кристаллических структур и описание наблюдающихся в них типов химической связи; интерпретация кристаллических структур (выяснение причин, определяющих строение того или иного кристаллического вещества) и их предсказание; изучение связи физических и химических свойств кристаллов с их структурой и характером химической связи.
Строение кристаллов обнаруживает исключительное разнообразие; будучи, например, довольно простым в случае алмаза, оно оказывается весьма причудливым и сложным в случае кристаллического бора. Как правило, каждому кристаллическому веществу присуща своя структура. Однако достаточно часто (например, NaCI и KCI, Вг2 и CI2) разные вещества имеют структуру, одинаковую с точностью до подобия (изоструктурные вещества). Такие вещества нередко образуют смешанные кристаллы (см. Изоморфизм). С др. стороны, одно и то же химическое вещество, будучи полученным при разных условиях, может иметь разное строение (полиморфизм).
Кристаллические структуры в К. делят на гомодесмические (координационные) и гетеродесмические. В первых все атомы объединены одинаковыми химическими связями, образующими пространственный каркас. Здесь нет группировок, которые можно было бы назвать молекулами. Гомодесмическую структуру имеют, например, алмаз, галогениды щелочных металлов. Однако гораздо чаще кристаллические вещества имеют гетеродесмическую структуру; её характерная черта — присутствие структурных фрагментов, внутри которых атомы соединены наиболее прочными (обычно ковалентными) связями. Эти фрагменты могут представлять собой конечные группировки атомов, цепи, слои, каркасы. Соответственно выделяются островные, цепочечные, слоистые и каркасные структуры. Островными структурами обладают почти все органические соединения и такие неорганические вещества, как галогены, O2, N2, CO2, N2O4 и др. Роль «островов» играют молекулы, поэтому такие кристаллы называются молекулярными. Часто в качестве «островов» выступают многоатомные ионы (например, сульфаты, нитраты, карбонаты). Цепочечное строение имеют, например, кристаллы одной из модификаций Se (атомы связаны в бесконечные спирали) или кристаллы PdCl2, в которых присутствуют бесконечные ленты:
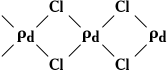
Слоистую структуру имеют графит, BN, MoS2 и др., каркасную структуру — CaTiO3 (атомы Ti и О, объединённые ковалентными связями, образуют ажурный каркас, в пустотах которого расположены атомы Ca). Известны гетеродесмические структуры, где имеются структурные фрагменты разного типа. Так, кристаллы комплексного соединения[N (CH3)4] [MnCI3] построены из «островов» — ионов [N (CH3)4] + и цепей
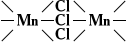
По характеру связи между атомами (в случае гомодесмических структур) или между структурными фрагментами (в случае гетеродесмических структур) различают: ковалентные (например, SiC, алмаз), ионные (см. Ионные кристаллы), металлические (металлы и интерметаллические соединения) и молекулярные кристаллы. Кристаллы последней группы, в которой структурные фрагменты связаны межмолекулярным взаимодействием, имеют наибольшее число представителей. Сюда, в частности, входят кристаллы инертных газов. Деление кристаллов на указанные группы в значительной мере условно, поскольку существуют постепенные переходы от одной группы к другой. Однако типичные представители разных групп существенно различаются по свойствам, в частности, по величине энергии структуры (работы, необходимой для разъединения одного моля кристаллического вещества, взятого при атмосферном давлении и комнатной температуре, на отдельные атомы, ионы или молекулы).