Эти «часы» состоят из сети белков, взаимно контролирующих синтез друг друга. В некоторых случаях они, прямо или косвенно, подавляют собственный синтез. Чтобы понять, как контролируемый синтез белков может превратиться в часы, стоит рассмотреть очень простую «игрушечную» систему. Она намного проще, чем в случае реальных сомитов: эта система состоит из одного-единственного гена, в последовательности которого закодирован белок, который синтезируется в момент активности гена и его же дезактивирует. Другими словами, белок подавляет собственный синтез. Будем считать, что подобный ген присутствует в клетках, так что работа основных биохимических процессов, связанных с синтезом белка, нам уже гарантирована. Напомним, что с активных генов сначала транскрибируются РНК – «копии». Затем с этой РНК в процессе трансляции синтезирует необходимый белок (глава 1).
Предположим, что процессы транскрипции и трансляции происходят за очень короткое время по сравнению со временем жизни РНК и молекул белка. Тогда в нашей системе-«игрушке» концентрация белка постепенно выйдет на стабильный уровень. Если в начале работы системы концентрация белка ниже этого уровня, активность гена не будет сильно подавляться. РНК будет синтезироваться и транслироваться, а концентрация белка при этом вырастет. Появится больше молекул белка, которые будут ингибировать активность гена, и производство новых белковых молекул будет снижаться до тех пор, пока не выйдет на уровень, позволяющий лишь компенсировать потерю белка, связанную с окончанием срока жизни молекул (рис. 25, а). Если же концентрация этого белка изначально слишком высока, работа гена будет подавляться, и новые белки не будут синтезироваться до тех пор, пока исходная концентрация белка не понизится за счет старения и распада молекул (рис. 25, б). Основная функция этой сетевой системы состоит в том, чтобы поддерживать концентрацию белка в четко заданных пределах. Для белков-долгожителей (срок их жизни измеряется в часах и днях) небольшое запаздывание в работе системы, связанное с паузами на транскрипцию и трансляцию (на них уходят минуты), не имеет большого значения. Такие системы используются клетками для поддержания количества отдельных молекул в пределах допустимого.

Рис. 25. Поведение системы, в которой белок (обозначен жирной линией) подавляет синтез собственной РНК (обозначена тонкой линией). В результате возникает запаздывание, незначительное по сравнению со временем жизни белка. Даже если исходная концентрация белка слишком низкая (а) или слишком высокая (б), она все равно придет к стабильному значению. Сравните этот рисунок с рис. 26
Если теперь предположить, что белок «живет» так недолго, что время, необходимое для его создания, сопоставимо со временем его жизни, поведение системы становится совершенно другим. Рассмотрим ситуацию, когда в нашей модельной системе концентрация белка очень низкая. В присутствии небольшого количества белка транскрипция гена не подавляется и может проходить быстро. С некоторым запаздыванием увеличивается концентрация РНК, а немного позже, по мере трансляции РНК, вырастет и концентрация белка. С увеличением числа молекул белка транскрипция гена подавляется, но, пока концентрация РНК достаточно высока, белок будет производиться за счет трансляции этой РНК до тех пор, пока она не деградирует. В результате концентрация белка превысит «пороговый» уровень (рис. 26). По-настоящему высокой концентрации белка достаточно, чтобы полностью выключить транскрипцию гена. По мере того как молекулы РНК и белка деградируют, концентрация белка уменьшится, и транскрипция начнется снова. Однако из-за запаздывания, связанного с транскрипцией и трансляцией, понадобится некоторое время, прежде чем концентрация белка начнет расти. Быстрое разрушение белка говорит о том, что его концентрация резко уменьшается и «пороговый» уровень опять будет перейден, но уже в обратном направлении. В системе опять становится слишком мало белка, а это значит, что цикл начнется снова. Запаздывания, связанные с транскрипцией и трансляцией, вызывают многократные резкие скачки системы: от низких значений концентрации к высоким. В результате вместо стабильности мы получаем чередование высоких и низких уровней концентрации белка. Это напоминает тиканье часов.
Сетевая система «часов сегментации» значительно сложнее, чем один белок, контролирующий собственный синтез.[91] Судя по всему, функциональное ядро этих часов основано на системе реакционных петель с отрицательной обратной связью (это означает, что их компоненты репрессируют сами себя), похожих на те, что уже были описаны. Они зависят от белков, время жизни которых коротко по сравнению со временем, которое затрачивается на транскрипцию и трансляцию, необходимые для их синтеза. В работу часов вовлечено большое количество белков. Они способствуют стабильной работе часов и «сверяют» часы соседних клеток. У мышей полный цикл «часов сегментации» занимает около двух часов. Одна фаза этого цикла дает разрешение любой клетке, находящейся в разрешающей зоне еще не сегментированной мезодермы (с низким содержанием FGF), принять участие в создании сомита. Идет чередование фаз. В короткую фазу часов («тик») клетки в окне с малым содержанием FGF могут стать клетками сомита. В долгую фазу («так») они не участвуют в образовании сомита, даже если находятся в пределах разрешающей зоны. Такое чередование означает, что у разрешающей зоны есть запас времени для продвижения к хвостовой части на длину сомита до того, как клетки, обнаружившие, что они находятся в этой зоне, смогут поучаствовать в создании сомита.
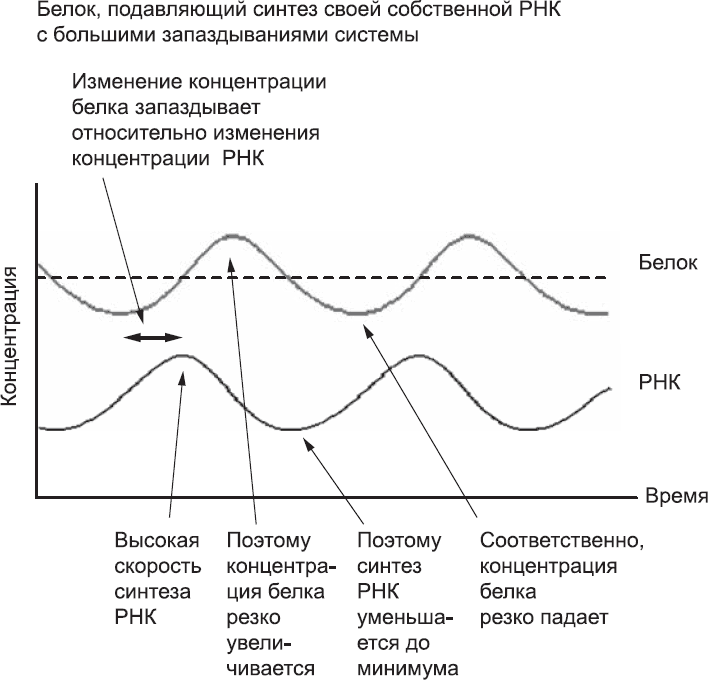
Рис. 26. Поведение системы, в которой белок подавляет синтез собственной РНК. Запаздывание в системе достаточно велико относительно времени жизни белка. В начале рассматриваемого периода исходно высокая концентрация белка понижается. При этом концентрация РНК низкая. Концентрация короткоживущих белков продолжает падать, и хотя на данный момент она и так слишком мала, чтобы ингибировать синтез РНК, понадобится довольно много времени для накопления РНК. Концентрация белка опускается ниже среднего уровня, и благодаря этому РНК синтезируется в больших количествах и аккумулируется. За счет повышения концентрации РНК концентрация белка тоже постепенно увеличивается и переходит средний уровень еще до того, как белку удается подавить синтез новой РНК. В этой модели скачки многократно повторяются. Так и создается некое подобие осциллятора, или «часов»
Затем мезенхима образует блоки, длина которых определяется протяженностью разрешающей зоны и частотой тиканья часов (рис. 27). Рассмотренный здесь механизм работы часов приводит к ряду интересных эффектов: если бы часы шли быстрее, разрешающая зона не продвинулась бы так далеко в хвостовую часть. Это привело бы к возникновению большего количества более мелких сомитов. У таких животных, как змеи, гораздо больше позвонков, чем у людей. Эмбрионы змей создают больше сомитов. Недавно ученые исследовали часы сегментации в эмбрионе змеи. Оказалось, что они работают гораздо быстрее, чем у мышей или людей. Все соответствует вышеизложенной теории.[92]
Четыре механизма действуют на локальном, клеточном, уровне. Производство ретиноевой кислоты, производство FGF, часы сегментации, рост эмбриона по направлению к хвосту – все это позволяет интегрировать пространство и время так, чтобы клетка могла «решить», участвовать ли ей в создании нового сомита. У клеток нет карты внутреннего строения эмбриона. Они даже не знают собственного места нахождения. Мы опять сталкиваемся с ситуацией, в которой клетки могут самоорганизоваться в сложно устроенные структуры достаточно большого пространственного масштаба, используя только набор локальных правил.