Итак, атом — это кристалл: кристаллическое ядро, возле которого в правильном порядке уложены электроны. Само ядро составлено из протонов и нейтронов, в свою очередь, образованных электронами и позитронами. Поэтому, скелет, остов атома, называемый "атомным ядром", — это, в конечном счёте, кристаллический комплекс из упорядоченно расположенных электронов и позитронов, которых почти поровну, как поровну ионов Na+ и Cl— в кристалле соли NaCl. Отрицательно заряженные электроны соединяются с положительно заряженными позитронами и — наоборот, взаимно нейтрализуясь. И лишь небольшой избыток позитронов придаёт ядру положительный заряд.
Заметим, что подобную модель строил ещё Ф. Ленард, считавший, что ядро имеет ажурную структуру [74] и образовано из "динамид", — попарно связанных элементарных отрицательных и положительных зарядов, — "электронов" и "позитронов", по-нынешнему. Масса атома пропорциональна числу образующих его динамид, поскольку складывается из их масс. Наличие в ядре в почти равной пропорции электронов и позитронов доказывают многие факты. Так, известно, что стабильны ядра с определённым соотношением числа протонов и нейтронов. При избытке протонов обычен β +-распад: ядро покидают избыточные положительные позитроны, находящиеся в протонах. Если же протонов не хватает, то ядро испытывает β —-распад: ядро покидают избыточные электроны, а содержавшие их нейтроны становятся протонами. Как видим, число электронов и позитронов должно быть сбалансировано. Электрон с позитроном могут покинуть ядро и вместе, — при облучении гамма-лучами, вырывающими из ядра пару e + e —. Как тут не вспомнить динамиды Ленарда — попарно связанные заряды в ядрах? Нет ничего удивительного, что подобным же образом представлял атом и другой физик, Ирвинг Ленгмюр, заложивший основы науки о плазме, — газе из положительных ионов и электронов. Да и автор первой модели атома, Дж. Томсон, открывший электроны, считал, что атом и его масса складывается из тысяч электронов и того же числа связанных с ними в пары положительных зарядов [139]. А, самое удивительное, что к таким взглядам за тысячи лет до нас пришли древние индийцы (особенно школа вайшешики во главе с атомистом Кáнадой), которые ещё до Демокрита создали учение об атомах и молекулах, считая их составленными из "диад", — попарно связанных стандартных точечных частиц, аналогичных электронам и позитронам ( Мюллер М. Шесть систем индийской философии. М., 1995). Так и в нашей модели бипирамидальный каркас, электронные слои и ответственную за спектр электрон-позитронную сетку атома формируют, вероятно, позитроны, прочно связанные с электронами в электродиполи, диады, или динамиды, обладающие весьма любопытными свойствами, например нулевой инерцией (§ 3.18). Оттого в атоме и нет позитронов в свободном состоянии.
Объясняет бипирамидальная модель ядра и открытую Планком связь энергии E= MV 2/2= hfи скорости Vэлектрона с частотой fего обращения в атоме. Магнитный момент, как нашли выше (§ 3.2), проявляется лишь на краях, рёбрах структур. Поэтому, рёбра бипирамиды аналогичны магнитным стержням. И, при соответствующей ориентации (Рис. 108) их магнитное поле в плоскости орбиты (с центром Oв вершине пирамид) будет перпендикулярно к этой плоскости и равно B=μ 0μ/π ar 2, где a— расстояние между электронами в стержне, равное их классическому радиусу r 0= e 2/4πε 0 Mc 2, μ=π eh/ M— их магнитный момент (§ 3.1). На электрон, летящий по орбите радиуса rс центром O, действует сила Лоренца F= eVB=e 2 fμ 0μ/ ar(с учётом значений Bи V=2π rf), направленная в Oи равная MV 2/ r. Откуда MV 2/2= feμ 0μ/ a, где eμ 0μ/ a= h. Именно эти электроны, запертые в магнитной ловушке атома, вылетают из него при облучении светом частоты f. Это объясняет планковский спектр излучения (§ 4.1), фотоэффект (§ 4.3) и эффект Комптона (§ 4.7). Итак, всего в атоме три типа электронов: одни сидят на гранях и перегородках ядра и генерируют линейчатый атомный спектр, другие уложены слоями в раструбах ядра, задавая химические свойства, а третьи, как на катушку, наматывают на ядро витки орбиты, отвечая за тепловой спектр и фотоэффект. Электроны легко переходят между этими тремя состояниями.
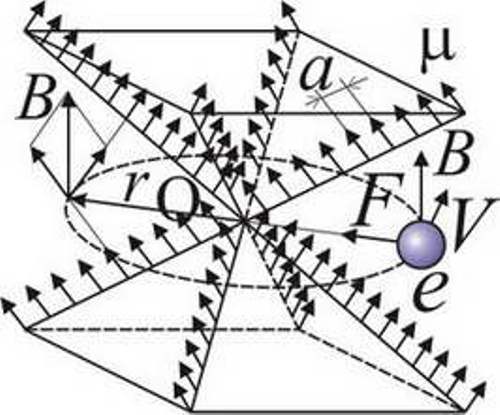
Рис. 108. Движение электрона в магнитном поле бипирамиды ядра с частотой f=E/h=MV 2/2h.
Предсказывает данная модель и такие свойства, которые не объяснила даже квантовая теория. Рассмотрим заполнение слоёв и связанные с этим физико-химические свойства. В первом периоде всё просто: в атоме водорода электрон занимает в слое № 1 одно из двух мест и, потому, атом может отдать электрон, либо принять на вакантное место чужой, проявляя валентности +I и — I. Гелий, в котором весь слой заполнен двумя электронами, не может ни отдать их, ни поглотить новые. То же — во 2-м и 3-м периоде: электроны заполняют второй и третий слой, имеющие по 8 мест, а атомы проявляют валентности, соответствующие числу электронов в слое. Завершают эти периоды благородные газы, где все 8 мест крайнего слоя заняты электронами, связанными в слое столь прочно, что уже не отрываются, придавая газам химическую инертность (Рис. 106).
В последующих, — 4-м и 5-м периодах важен уже порядок заполнения слоя. Сперва электроны заполняют слой по периметру, где они удерживаются крепче (совсем как лёд начинает кристаллизоваться сперва по краям водоёма). Таких крайних мест всего 10, соответственно, и элементов этого типа в периодах по 10,— с калия по никель и — с рубидия по палладий. Когда периметр заполнен, прочно связанные в нём электроны отрываются лишь с большим трудом (Рис. 109). Поэтому, от заполнения периметра у никеля и палладия (а также у платины в 6-м периоде) эти благородные металлы по инертности становятся аналогичны благородным газам. А, при дальнейшем заполнении слоя, отсчёт групп и валентностей начинается заново, подобно тому, как это происходит во 2-м и 3-м периодах после завершения слоёв у инертных газов. Свойства элементов потому и повторяют друг друга, что электроны, расположенные в завершённых слоях или целиком занявшие периметр, не отрываются и не участвуют в образовании связей, а оставшиеся электроны образуют конфигурации, подобные конфигурациям предшествующих элементов.
В 6-м и 7-м периодах возникают группы лантаноидов (La — Lu) и актиноидов (Ac — Lr), содержащие по 15 химически подобных элементов с валентностью +III, разом помещаемых в IIIБ группу своего периода [145]. Такое число элементов есть следствие того, что электроны из периметра слоя крепко в нём связаны и мало влияют на свойства атома. А, потому, элементы, у которых идёт заполнение 14-ти мест этого периметра (у La периметр пустой), — химически подобны. После того, как периметр заполнен, дальнейшее заполнение слоя идёт так же, как у слоёв 4-го и 5-го периодов.
В лице лантаноидов и актиноидов квантовая физика имеет массу нерешённых проблем. Так, известно, что элементы эти способны проявлять, помимо валентности +III, и другие, — совершенно необъяснимые. А, с позиций пирамидальной модели, они естественны: электроны периметра, хоть и с трудом, всё же могут отрываться, — тогда атом проявляет соответствующие степени окисления. Кроме того, если полость каждой пирамиды разделена перегородкой пополам (Рис. 107), и периметр заполняется сначала в одной полости, а затем в другой, то электроны периметра можно разбить на две равных группы по 7 электронов в каждой. Электроны, занявшие все семь мест, оказываются крепко связаны и, потому, не влияют на химические свойства. Соответственно, элементы образуют два подпериода, расположенные один под другим в таблице Менделеева (Рис. 109). Именно такую форму придал некогда таблице Менделеев, а поздней она была уточнена его другом и коллегой, чешским химиком Б.Ф. Браунером [145]. Этот исконный вариант таблицы сразу объясняет, как элементы Ce и Tb могут иметь валентность (+IV), а Eu и Yb — валентность (+II): они просто попадают в 4-ю и 2-ю группы. Элементы же La, Gd и Lu, стоящие в третьей группе, проявляют всегда только валентность +III. Впрочем, из-за того, что электроны могут образовывать в атоме разные конфигурации, валентность может быть различной (§ 4.14).