Точно также происходит растворение в воде твердых веществ. Сначала, уткнувшись своим консольным лепестком в атом (или молекулу) твердого вещества, молекула воды производит инъекцию электронов (шприцует их); электроны ослабляют межатомные связи вещества; а затем ударами своих лепестков, как дубинами, вода срывает непрочные атомы и молекулы со своих мест и поглощает их. Растворение в воде кислот, содержащих кислород, сопровождается диссоциацией, то есть частичным или полным отделением атомов водорода.
Приблизительно также происходит окисление металлов. Сначала инъекцией электронов и ударами своих лепестков атомы кислорода, растворенные в воде, ослабляют крепление поверхностных атомов металла, а затем обволакивают их своими лепестками как щупальцами; при этом присасывающие желоба кислорода накладываются на присасывающие желоба металла и нейтрализуют их. Точно также ведет себя по отношению к металлу кислород, находящийся в составе кислот. Соединение их между собой происходит с помощью желобов, поэтому их количественное соотношение определяется соотношением длин желобов, и оно может быть некратным; отсюда — переменная и дробная валентность.
Обволакивание атомов различных химических элементов с помощью щупальцев (лепестков) воды способствует успокоению пульсаций ее молекул: их колебания амортизируются соседними атомами. Лишившись своей подвижности, молекулы воды становятся средствами скрепления других атомов, то есть клеем как азот, как углерод, как бор или бериллий в подобной роли. Поэтому в минералах оказывается так много воды.
Среди петлевых соединений кислорода можно выделит образование угарного и углекислого газов. При недостатке кислорода его атомы в первую очередь соединяются своими петлями с выкрученными петлями атомов углерода; его нормально замкнутые петли при этом не раскрываются; это — угарный газ. При избытке кислорода и при высокой температуре замкнутые петли углерода также раскрываются и соединяются с петлями других атомов кислорода; возникает углекислый газ. В указанных соединениях напряженность атомов углерода и кислорода уменьшается, то есть уменьшается их потенциальная энергия, и соответственно увеличивается кинетическая, тепловая энергия. Повышение температуры сопровождается выделением света: светятся атомы углерода.
Из трех состояний кислорода: атомарного, молекулярного и озонного, — последнее — наиболее активное. Если у одиночного атома кислорода и молекулы парные лепестки замкнуты своими петлями и не совсем готовы для присоединения к другим атомам, то у озона они находятся в непрочном соединении между собой и легко раскрываются.
4.9. Фтор
Фтор — девятый по счету химический элемент таблицы Менделеева, его атомная масса равна 18,998. Он представляет собой бледно-желтый газ с температурой плавления минус 219,6 и кипения минус 188,1 градусов Цельсия.
Фтор — самый сильный окислитель, он окисляет даже кислород; его химическая активность настолько высока, что он реагирует почти со всеми веществами, за исключением инертных газов: гелия, аргона, неона; при нормальных условиях он не взаимодействует также с азотом и с углеродом в алмазной модификации. При реакциях с его участием выделяется много тепла, иногда это происходит в виде взрыва.
Странное дело, углефторовые соединения — фторопласт и тефлон — отличаются, наоборот, поразительной химической стойкостью: их не берет даже царская водка — концентрированная смесь азотной и соляной кислот. Инертностью отличаются также фреоны (хладоны) — насыщенные углеводороды, в которых водород заменен на фтор и хлор; фреоны являются газами и используются в качестве хладоагентов для холодильников; их температура кипения — около минус 30 градусов Цельсия.
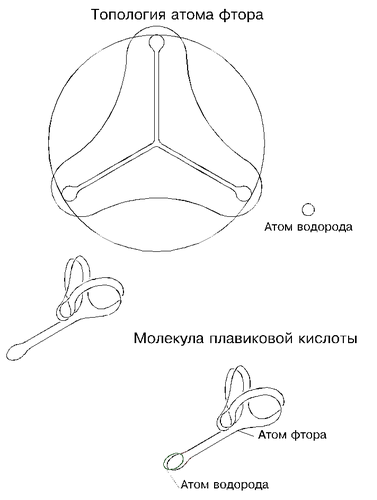
Из других соединений широко известны плавиковая кислота, молекула которой состоит из одного атома углерода и одного атома фтора, и природные минералы: флюорит, плавиковый шпат и другие. Свободный фтор в природе не встречается.
Топология атома фтора завершает треугольную тему. После формирования из исходного тора трехлучевой звезды процесс дальнейшего развития атома выбирает иное, чем у азота и кислорода, направление: два лепестка (луча) успевают сблизиться своими концами, на которых расположены присасывающие петли, раньше, чем, сойтись своими основаниями; сблизившиеся петли разворачиваются и слипаются, нейтрализуя друг друга; слипшиеся петли изгибают дугой свои спаренные шнуры и ловят макушками желоб оставшегося одиночного лепестка. В законченном виде атом фтора напоминает летящего гуся с крыльями из завернувшихся лепестков и с вытянутой шеей последнего третьего из них; петля на конце третьего лепестка ассоциируется с клювом, готовым ущипнуть. Отличие от принятого образа будет состоять, скорее всего, в том, что голова гуся не вытянута в струнку, а мечется из стороны в сторону. Новое, фторовское направление в формировании атома обусловлено удлинением лепестков: у фтора они длиннее приблизительно на 1000 эфирных шариков, чем у кислорода, и на 1500, чем у азота, а вся длина шнура атома фтора составляет 35 000 шариков.
Повышенная активность атома фтора объясняется тем, что он, во-первых, может накапливать на своих присасывающих желобах электронов больше, чем даже атомы кислорода (за счет более длинных желобов, на которых может скопится более 17 000 электронов), а во-вторых, весь этот запас электронов приходится не на два щупальца как у кислорода, а на один клюв. Имея очень длинную шею, атом фтора может дотянуться до самых удаленных слипшихся участков в молекулах других веществ, выбросить на них большую порцию электронов, ослабив тем самым их связи, прилипнуть своей петлей или своим желобом к столкнувшимся атомам или молекулам и образовать новое соединение. Поэтому перед агрессией фтора не может устоять практически ни одно вещество, и поэтому оно называется разрушителем (по гречески «фторос» — разрушение). К слову, разъединительное влияние электронов сказывается и на соединениях самого фтора: если пропустить через плавиковую кислоту электрические разряды, она распадается на водород и фтор.
С другой стороны, удивительную химическую инертность фторопласта и тефлона можно объяснить тем, что в соединениях атомов фтора с атомами углерода нейтрализуются (закрываются) не только присасывающие стороны их петель, но и их присасывающие желоба: и у того и у другого длина каждого из желобов составляет приблизительно 5000 эфирных шариков, поэтому они смыкаются без остатка. Между собой молекулы тетрафторэтилена, образующие фторопласт и тефлон, контактируют отдельными точками, в частности боковушками петель; эти контакты не очень прочны.
С азотом фтор не соединяется по простой причине: молекула азота, как мы знаем, полностью закрыта, и атом фтора бессилен подобрать к ней ключи; к тому же молекула не очень боится его электронных инъекций: у нее у самой имеется большое количество электронов. Также нам должно быть понятно то, что атом фтора не способен разрушить кристаллы алмаза: они так крепко сшиты, что не имеют щелей и прорех, через которые он мог бы проникнуть своим клювом; самое большое, что способен сделать фтор с алмазом, так это прилипнуть к нему, но и это возможно только в том случае, если поверхностные связи кристалла случайно окажутся незавершенными.
В качестве хладоагентов соединения фтора применяют потому, что они имеют очень удобную температуру кипения: давлением компрессора и охлаждением их легко превращать в жидкость, а она, испаряясь, отбирает тепло. К тому же теплоемкость фтора, атом которого имеет консоль, то есть длинную шею, довольно большая. Она — эта теплоемкость — является причиной того, что все реакции с участием фтора идут с выделением тепла: успокаиваясь в соединениях с другими атомами, фтор передает вновь образованным молекулам все свои тепловые движения.