Есть среди них скромные кристаллы каменной соли – природного хлористого натрия, т.е. обычной поваренной соли. Они встречаются в природе в виде прямоугольных параллелепипедов или кубиков. Простая форма и у кристаллов кальцита – прозрачных косоугольных параллелепипедов. Куда сложнее кристаллы кварца. У каждого кристаллика множество граней разной формы, пересекающихся по ребрам разной длины.
Однако кристаллы – совсем не музейная редкость. Кристаллы окружают нас повсюду. Твердые тела, из которых мы строим дома и делаем станки, вещества, которые мы употребляем в быту, – почти все они относятся к кристаллам. Почему же мы этого не видим? Дело в том, что в природе редко попадаются тела в виде отдельных одиночных кристаллов (или, как говорят, монокристаллов). Чаще всего вещество встречается в виде прочно сцепившихся кристаллических зернышек уже совсем малого размера – меньше тысячной доли миллиметра. Такую структуру можно увидеть лишь в микроскоп.
Тела, состоящие из кристаллических зернышек, называются мелкокристаллическими, или поликристаллическими («поли» – по-гречески «много»).
Конечно, к кристаллам надо отнести и мелкокристаллические тела. Тогда окажется, что почти все окружающие нас твердые тела – кристаллы. Песок и гранит, медь и железо, салол, продающийся в аптеке, и краски – все это кристаллы.
Есть и исключения; стекло и пластмассы не состоят из кристалликов. Такие твердые тела называются аморфными.
Итак, изучать кристаллы – это значит изучать почти все окружающие нас тела. Понятно, как это важно.
Одиночные кристаллы сразу же узнают по правильности форм. Плоские грани и прямые ребра являются характерным свойством кристалла; правильность формы несомненно связана с правильностью внутреннего строения кристалла. Если кристалл в каком-то направлении особо вытянулся, значит, и строение кристалла в этом направлении какое-то особенное.
Но представьте себе, что из крупного кристалла на станке изготовлен шар. Удастся ли сообразить, что в руках у нас кристалл, и отличить этот шар от стеклянного? Естественная форма кристалла показывает, что кристалл различен в разных направлениях. Если это различие проявляется в отношении формы, то оно должно существовать и в отношении других свойств. Прочность кристалла, электрические его свойства, проводимость тепла – все свойства могут различаться в разных направлениях. Эта особенность кристалла называется анизотропией его свойств. Анизотропный – это значит разный в разных направлениях.
Кристаллы анизотропны. Напротив, аморфные тела, жидкости и газы изотропны, т.е. обладают одинаковыми («изо» – по-гречески «одинаково») свойствами в разных направлениях («тропос» – направление).
Анизотропия свойств и позволяет узнать, является ли прозрачный бесформенный кусочек вещества кристаллом или нет.
Строение кристаллов
Почему так красива, правильна форма кристалла? Грани его, блестящие и ровные, выглядят так, словно над ними поработал искусный шлифовальщик. Отдельные части кристалла повторяют одна другую, образуя красивую симметричную фигуру.
Ответ на поставленный вопрос может быть лишь один – внешней красоте должна отвечать внутренняя правильность. Эта правильность заключается в многократном повторении одних и тех же основных частей.
Представьте себе парковую решетку, сделанную из прутьев разной длины и расположенных как попало. Безобразная картина. Хорошая решетка построена из одинаковых прутьев, расположенных в правильной последовательности на одинаковых расстояниях один от другого.
Такую же самоповторяющуюся картину мы находим в обоях. Здесь элемент рисунка – скажем, девочка, играющая в мяч, – повторяется уже не в одном направлении, как в парковой решетке, а заполняет плоскость.
Какое же отношение имеют парковая решетка и обои к кристаллу? Самое прямое. Парковая решетка состоит из звеньев, повторяющихся вдоль линии, обои – из картинок, повторяющихся вдоль плоскости, а кристалл – из групп атомов, повторяющихся в пространстве. Поэтому и говорят, что атомы кристалла образуют пространственную (или кристаллическую) решетку.
В настоящее время известно строение многих сотен кристаллов. Расскажем про строение простейших кристаллов и прежде всего тех, которые построены из атомов одного сорта.
Наиболее распространены три типа решеток. Они показаны на рис. 89. Точками изображены центры атомов; линии, объединяющие точки, не имеют реального смысла. Они проведены лишь для того, чтобы сделать читателю более ясным характер пространственного расположения атомов.
Рис. 89, аи 89, бизображают кубические решетки. Чтобы представить себе эти решетки яснее, вообразите, что вы сложили простейшим способом – ребро к ребру, грань к грани – детские кубики.
Если теперь мысленно разместить точки по вершинам и центрам объемов кубов, то возникнет кубическая решетка, изображенная на левом рисунке. Такая структура называется кубической объемноцентрированной. Если разместить точки по вершинам кубов и в центрах их граней, то возникнет кубическая решетка, изображенная на среднем рисунке. Она называется кубической гранецентрированной.
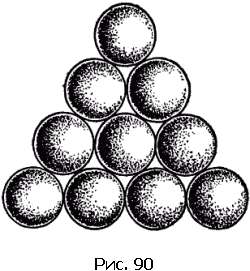
Третья решетка (рис. 89, в) называется плотнейшей гексагональной (т.е. шестиугольной). Чтобы понять происхождение этого термина и яснее представить себе расположение атомов в этой решетке, возьмем биллиардные шары и начнем укладывать их как можно плотнее. Прежде всего составим плотный слой – он выглядит так, как биллиардные шары, собранные «треугольником» перед началом игры (рис. 90). Отметим, что шар внутри треугольника имеет шесть соприкасающихся с ним соседей, и эти шесть соседей образуют шестиугольник. Продолжим укладку наложением слоев друг на друга. Если поместить шары следующего слоя непосредственно над шарами первого слоя, то такая упаковка была бы неплотной. Стараясь разместить в определенном объеме наибольшее число шаров, мы должны положить шары второго слоя в лунки первого, третьего слоя – в лунки второго и т.д. В гексагональной плотнейшей упаковке шары третьего слоя размещены так, что центры этих шаров лежат над центрами шаров первого слоя. Центры атомов в гексагональной плотнейшей решетке расположены так, как центры шаров, плотно уложенных описанным способом.
В описанных трех решетках кристаллизуется множество элементов:
Гексагональная плотнейшая упаковка..... Be, Co, Hf, Ti, Zn, Zr
Кубическая гранецентрированная........ Al, Cu, Co, Fe, Au, Ge, Ni, Ti
Кубическая объемноцентрированная ...... Cr, Fe, Li, Mo, Ta, Ti, U, V
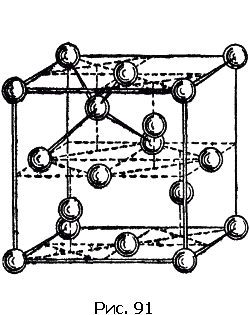
Из других структур упомянем лишь немногие. На рис. 91 изображена структура алмаза. Для этой структуры характерно то, что атом углерода алмаза имеет четыре ближайших соседа. Сопоставим это число с соответствующими числами описанных только что трех наиболее распространенных структур. Как видно из рисунков, в плотнейшей гексагональной упаковке у каждого атома 12 ближайших соседей, столько же соседей у атомов, образующих гранецентрированную кубическую решетку; в объемноцентрированной решетке у каждого атома 8 соседей.
Несколько слов скажем о графите, строение которого показано на рис. 92. Особенность этой структуры бросается в глаза. Графит состоит из слоев атомов, причем атомы одного слоя связаны между собой сильнее, чем атомы соседних слоев. Это связано с величиной межатомных расстояний: расстояние между соседями в одном слое в 2,5 раза меньше кратчайшего расстояния между слоями. Наличие слабо связанных атомных слоев приводит к тому, что кристаллы графита легко расщепляются вдоль этих слоев. Поэтому твердый графит может служить смазочным материалом в тех случаях, когда невозможно применять смазочные масла, – например, при очень низких или очень высоких температурах. Графит – твердый смазочный материал.