Вернер Гейзенберг (рис. 17.3) работал в Геттингенском университете в группе, которой руководил Макс Борн (1882–1970), занятый изучением странного поведения электронов в атоме. В июне 1925 года в воздухе витал оптимизм: все ждали прорыва. Но именно тогда у Гейзенберга случился сильный приступ сенной лихорадки, вынудивший его уехать из Геттингена. Он отправился путешествовать по суровому острову Гельголанд в Северном море, где его сенная лихорадка прошла. Там 23-летний Гейзенберг продолжал думать о работе. Наконец все сошлось, и родилось точное математическое описание поведения электрона. Позже Гейзенберг рассказал, что как-то под утро, в три часа…
«Я уже не сомневался в логике и стройности той части квантовой механики, которой касались мои вычисления. Вначале я был очень встревожен: я чувствовал, что смотрю сквозь поверхности атомных явлений в их странную и прекрасную суть, и у меня кружилась голова оттого, что я могу исследовать эти математические структуры, природа которых великодушно раскрылась предо мной».
После возвращения в Геттинген Гейзенберг постеснялся рекламировать свое открытие. Он описал результаты в научной статье и дал копии рукописи Борну и своему другу из Мюнхена Вольфгангу Паули. Борн послал статью в журнал Zeitschrift filr Physik («Физический журнал») для публикации. Гейзенбергу нужно было уехать, и он оставил Борна размышлять над смыслом таблиц в этой статье.
Рис. 17.3. (а) Вернер Гейзенберг (1901–1976) и (6) Эрвин Шрёдингер (1887–1961).
Борн обратил внимание, что таблицы Гейзенберга были матрицами — основными величинами раздела математики, называемого матричной алгеброй. Вместе со своим коллегой Паскуалем Иорданом Борн начал переводить теорию Гейзенберга на язык матриц. Сам Гейзенберг, бывший в то время в Копенгагене, принял участие в завершении этой теории. Примерно тогда же Поль Дирак в Кембридже создал такую же теорию, но в иной математической форме, а через год Эрвин Шрёдингер разработал еще один вариант (о нем мы расскажем ниже). Для квантовой физики это была бурная эпоха!
Расплывчатые частицы: принцип неопределенности Гейзенберга.
Главная особенность квантовой механики заключена в ее вероятностной природе, сформулированной Максом Борном в 1926 году. Вместо того чтобы говорить о точных значениях физических величин, есть возможность описать только распределение вероятности этих значений. Связано это с принципом неопределенности, опубликованным Гейзенбергом в 1927 году. Гейзенберг понял, что одновременное существование частицы как материального тела и как волны требует фундаментальных ограничений в положении частицы. Невозможно сказать, на каком расстоянии от атомного ядра расположен электрон в данный момент времени. Одновременно знать об этих двух вещах невозможно. Электрон «размазан» по окрестности ядра. Можно только сказать, что наиболее вероятно обнаружить электрон на таком-то расстоянии и в таком-то направлении, а не на других расстояниях и не в других направлениях. В этом смысле «планетные орбиты» из простой модели Бора теперь представляют только наиболее вероятные области, где можно найти электрон. Это касается не только электрона, связанного в атоме, но и всех электронов и вообще всех частиц. Общее правило гласит: частица «размазана» тем сильнее, чем она легче. «Размазанность» обычных предметов, типа теннисного мяча, совершенно незаметна.
«Размазанность частицы» — звучит абстрактно, но на деле имеет конкретные следствия. Например, при испускании альфа-излучения частица выходит из радиоактивного ядра путем туннелирования. Альфа-частица связана с ядром сильным ядерным взаимодействием, надежно удерживающим ее в ядре. Но мы видим, как время от времени альфа-частицы покидают ядро. Георгий Гамов (изучавший также космологию и генетический код; см. главы 24 и 28), используя квантовую теорию, объяснил это тем, что альфа-частицы «размазываются» не только по ядру, но и выходят немного за его пределы. «Размазывание» означает, что с некоторой вероятностью частицу можно обнаружить в любом месте той области, по которой она «размазана». Следовательно, альфа-частица находится внутри ядра с вероятностью немного меньше 100 %, и в то же время она с небольшой вероятностью находится вне ядра. Поэтому время от времени положительно заряженная альфа-частица материализуется вне ядра, вне области сильного ядерного взаимодействия, где электрическое отталкивание от положительно заряженного ядра выталкивает ее наружу.
На эффекте туннелирования основан и синтез гелия в недрах Солнца, дающий такой любимый нами солнечный свет. Ядра гелия образуются при объединении ядер водорода — протонов, которые должны сблизиться настолько, чтобы их связало сильное ядерное взаимодействие. Сближению протонов мешает их электрическое отталкивание, преодолеть которое протоны могли бы при очень высокой скорости движения. Но в недрах Солнца их скорости довольно малы. Как же разрешается эта дилемма? Поскольку протоны тоже «размазаны» вблизи своего среднего положения, временами они материализуется ближе друг к другу, чем на это указывает их среднее положение. Так что протоны, к своему удивлению, вдруг могут оказаться в области сильного ядерного взаимодействия, хотя ожидать этого было невозможно.
Рассмотрим теперь такой случай. Мы сильно бьем в кирпичную стену дома теннисным мячом. Неожиданно мяч проходит сквозь стену и оказывается внутри здания. А в стене как не было дырки, так и нет; мяч туннелировал сквозь стену. То, что этого никогда не может произойти, обусловлено большой массой теннисного мяча по сравнению с массой протона! Теперь понятно, почему электрон не может быть составной частью ядра. Как легкая частица, электрон размазан по такой большой области, что не может удержаться в ловушке внутри ядра.
Структура атомов.
Развитие квантовой теории позволило понять структуру атома: почему атомы каждого элемента обладают характерными химическими свойствами, как атомы объединяются в химические соединения и многое другое. Вычисления в квантовой механике основаны на уравнении Шредингера, выведенном в 1926 году австрийцем Эрвином Шрёдингером, работавшим тогда в Цюрихе (см. рис. 17.3). Поскольку тогда уже было ясно, что электроны можно рассматривать как волны, Шредингер представил электроны в атомах как колебательное явление. Он показал, что только определенные виды колебаний могут длиться долго, как у музыкального инструмента с долго звучащей отдельной нотой. «Ноты» в атоме соответствуют электронным орбитам Бора (рис. 17.4).
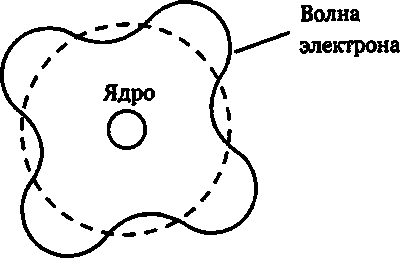
Рис. 17.4. Волны электронов, циркулирующие вокруг атомного ядра. Если на одном обороте укладывается целое число волн, то волна усиливается и возникает разрешенная электронная орбита. Если фазы волны после одного оборота не совпадают, интерференция приводит к их затуханию. Поэтому в модели Бора такой орбитальный радиус невозможен.
Модель Бора для атома водорода далее была развита в оболочечную модель атома, которая объясняет периодическую систему элементов. Вместо предложенных Бором орбит мы сейчас говорим об оболочках атома. Элементы тяжелее водорода имеют несколько электронов, находящихся в разных оболочках. Но электроны не могут свободно выбирать оболочку, в которой они могли бы находиться; в наиболее спокойном состоянии оболочки атома заполняются электронами снизу вверх (от ядра наружу), до тех пор, пока все электроны не найдут свое место. Химические свойства определяются уровнем заполнения самой внешней оболочки. Атомы пытаются до конца заполнить свою внешнюю оболочку, захватывая электроны у соседей или используя электроны совместно с ними. Это приводит к химическим связям. У химически инертных благородных газов внешняя оболочка заполнена, поэтому им не требуется соединение с другими атомами.
Например, связь двух атомов водорода, позволяющая существовать молекуле водорода, основана на совместном использовании двух электронов обоими атомами. Это называется ковалентной химической связью, ее открыли в 1927 году немецкие физики Вальтер Гайтлер и Фриц Лондон. Ковалентная связь играет важную роль в сложных молекулах, таких, на которых основана жизнь (мы обсудим структурные элементы жизни в части IV). Причина в том, что каждый атом при этом может иметь несколько связей с другими атомами, по-разному ориентированными относительно него. К тому же ковалентная связь очень крепкая. Особенно важны атомы углерода, у которых не хватает четырех электронов во внешней оболочке. Атомы углерода заполняют свою внешнюю оболочку разными способами, которые могут давать сложные цепочки атомов с прочными связями (рис. 17.5).