Для приготовления дефибринированной крови наиболее часто используют трикалевую (дикалевую) соль этилендиаминтетрауксусной кислоты (ЭДТА), тринатрий-цитрат и гепарин. Первые два вещества ингибируют коагуляцию путем удаления кальция из крови.
Из известных антикоагулянтов 1-й фазы свертывания наибольшее физиологическое значение имеют ингибитор активированного фактора ХI (ХIа), относящийся к α-2-глобулинам, и антитромбопластины (ингибиторы комплекса фактор III – фактор VIIа). К ингибиторам 2-й фазы коагуляции относится антитромбин II – α-2-глобулин крови; ингибирует не только тромбин, но и другие активированные факторы свертывания – Ха, IХа, ХIа, ХIIа, калликреин. На антитромбин III приходится большая часть спонтанной антикоагулянтной активности, что определяет его ведущую роль в поддержании жидкого состояния крови и предупреждении тромбозов. Доля других естественных антитромбинов – α-2-макроглобулина и α-1-антитрипсина – составляет лишь около 25% антикоагулянтной активности дефибринированной плазмы крови.
Фибринолиз осуществляется протеолитической ферментной системой крови – плазмогеплазмином. Превращение плазминогена в активную форму происходит с помощью активаторов, которые находятся в плазме крови, моче, различных тканях, образуясь в эндотелии сосудов. Обнаруживаемый в моче активатор (урокиназа) продуцируется почкой. Способностью активировать плазминоген обладают и некоторые продукты бактериального происхождения, в частности стрептокиназа.
Под влиянием активаторов происходит ферментативное расщепление молекулы плазминогена, и образуется плазмин, обладающий выраженным протеолитическим свойством в отношении фибрин-фибриногена (кроме того, факторов VII, V, комплемента, некоторых гормонов). Лизис фибриногена происходит в несколько этапов. Вначале после отделения мелких фрагментов А, В, С формируется высокомолекулярная Х-фракция. Затем она расщепляется на D- и Y-фракции. В дальнейшем Y-фракция расщепляется на вторую D- и дополнительную Е-фракцию. D- и Е-фракции – это конечные продукты деградации фибриногена. Деградация плазмином растворимого фибрина сходна с таковой фибриногена, за исключением того, что на первом этапе отсутствуют мелкие фрагменты. Деградация стабилизированного фибрина отличается образованием вместо D-фракции двойного по размеру фрагмента-D-димера.
Ферментативный фибринолиз поддерживают комплексные соединения гепарина с фибриногеном, адреналином, мочевиной, плазмогеном, обладающие способностью лизировать нестабилизированные сгустки фибрина (неферментативный фибринолиз). Фибрин может лизироваться протеазами, выделяемыми лейкоцитами, которые участвуют в фибринолизе также благодаря освобождению лейкоцитарных активаторов плазминогена и фагоцитозу продуктов расщепления фибрина.
Терапевтическую стимуляцию фибринолиза проводят с помощью ферментов бактериального происхождения (стрептокиназы и др.) или урокиназы.
Представление о фибринолитической активности крови дает ее определение эуглобулиновым методом. Метод Ковальского – осаждение в кислой среде и при низкой температуре эуглобулиновой фракции, содержащей факторы свертывания крови и фибринолиза, главным образом плазминоген. 0,1 мл оксалатной плазмы (1 : 9) помещают в центрифужную пробирку, добавляют 1,8 мл кислой воды (рН 5,2), пробирку ставят в холодильник при 4 °С (при этом из плазмы выпадает эуглобулиновая фракция). Через 30 мин пробирку вынимают и центрифугируют в течение 10 мин при 2000 об./мин. Надосадочную жидкость отсасывают, к осадку приливают 0,1 мл бората натрия и ставят в термостат при 37 °С на несколько минут до полного растворения осадка. Добавляют 0,1 мл раствора хлорида кальция (содержащийся в эуглобиновой фракции фибриноген превращается в фибрин). Засекают время образования сгустка и ставят пробирку в термостат до полного лизиса сгустка. Время от момента образования сгустка до его растворения выражает фибринолитическую активность крови, которая в норме равна 3–4 ч.
Применяют методы исследования фибринолиза, основанные на дополнительной стандартизированной активации его стрептокиназой, а также методы выявления в плазме крови продуктов фибринолиза – ПДФ (иммунологические и химические) и их соединений с фибрин-мономерами и фибриногеном (паракоагуляционные пробы), методы исследования неферментативного фибринолиза по Б. А. Кудряшову.
Анализаторы свертывания крови
В лабораторной практике широко применяются коагулологические анализаторы, действующие в автоматическом и полуавтоматическом режиме.
Коагулометры лабораторные, автоматические и полуавтоматические. Применяются для качественного и количественного определения одного или нескольких факторов коагуляции, задействованных в гемостазе. В частности, может быть определено тромбиновое, частичное тромбопластиновое время. Принцип работы может быть основан на нескольких методах: спектрофотометрии, турбидиметрии, нефелометрии, электрометрии, механическом средстве контроля образования сгустка.
Приборы данного типа отличаются высокой производительностью и точностью полученных результатов. Для их работы требуется минимальное количество биологического материала. При работе с полуавтоматическими и автоматическими приборами исключается человеческий фактор (вероятность ошибки).
Иммунологические реакции
Иммунологические реакции используются для выявления специфических антител, идентификации возбудителей и других антигенов, определения групп крови и подбора адекватного донора при пересадках органов и тканей. Серологические реакции – реакции между антигенами и антителами in vitro – применяют для выявления неизвестного антигена или антитела с помощью известного антитела или антигена соответственно. Корпускулярные антигены дают феномен агглютинации, растворимые – преципитации. В лабораторной практике используют реакции агглютинации, преципитации, связывания комплемента и др.
Антигены, по которым отдельные индивидуумы или группы особей одного вида различаются между собой, являются изоантигенами. Изоантигены, генетически связанные, объединены в группы, получившие следующие названия: система АВО, резус и др. В плазме человека всегда содержатся естественные, полные, холодовые изоантитела к агглютиногенам А и В. Агглютинин анти-А – α-агглютинин, а агглютинин анти-В – β- агглютинин (табл. 6).
Таблица 6
Групповая принадлежность людей по системе АВО
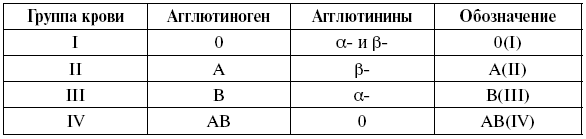
Определение группы крови (определение агглютиногенов). Реакцией агглютинации с помощью стандартных сывороток определяют групповые агглютиногены в эритроцитах. Ампулы или флаконы со стандартными сыворотками двух различных серий каждой группы ставят в 2 штатива, имеющих по 3 гнезда, или в 1 штатив с двумя рядами гнезд. Слева направо ставят сыворотки групп 0 α-β (I), А β(II), В α(III). Отдельно ставят сыворотку АВ0(IV). Определение производят на белых пластинах или тарелках. На левой стороне делают надписи 0 α-β, в середине – А β, справа – В α. Под соответствующей надписью наносят по 0,1 мл каждой стандартной сыворотки отдельной для каждой сыворотки пипеткой. Кровь для исследования берут из пальца, 0,01 мл крови сухой стеклянной палочкой наносят рядом с каждой каплей стандартной сыворотки. Перемешивают капли стандартной сыворотки с исследуемой кровью. После этого пластину покачивают, затем на 1–2 мин оставляют в покое и снова периодически покачивают. Наблюдение за ходом реакции проводят не менее 5 мин, несмотря на то что агглютинация начинается в течение первых 10–30 с, так как возможна поздняя агглютинация, например эритроцитами группы А2 (II). По мере наступления агглютинации, но не ранее чем через 3 мин, в те капли, в которых наступила агглютинация, добавляют изотонический раствор хлорида натрия и продолжают наблюдение при покачивании пластинки в течение 5 мин, после чего оценивают результат. При положительной реакции в смеси появляются видимые невооруженным глазом мелкие красные зернышки (агглютинанты), состоящие из склеенных эритроцитов. При этом сыворотка полностью или частично обесцвечивается. В случае отрицательной реакции на протяжении всего времени наблюдения (5 мин) жидкость остается равномерно окрашенной в красный цвет и в ней не обнаруживаются агглютинанты. Результаты реакции в каплях с сыворотками одной группы обеих серий должны быть одинаковыми. Возможны различные комбинации реакций: