Рис. 9.2. Сравнение эффекта нейтронного облучения на число хромосомных аберраций в клетках печени мышей и их возрастных изменений [22]. При однократном облучении дозой 192 рад аберрации наблюдаются в среднем) в 56 % клеток (треугольники)
Кларк и Рубин [17] изучили действие рентгеновского излучения на продолжительность жизни бабочки Habrobracon, у которой самки диплоидны, а самцы либо диплоидны, либо гаплоидны. Интактные самцы, как диплоидные, так и гаплоидные, имеют одинаковую продолжительность жизни. Однако гаплоидные особи более чувствительны к проникающей радиации, чем диплоидные. Это показывает, что соматическая мутация не может быть причиной старения; если бы это было так, то диплоидные особи имели бы большую продолжительность жизни, а диплоидные самцы и самки имели бы одинаковую продолжительность жизни. Диплоидные самцы более устойчивы к радиации. Это говорит о том, что повреждение, вызываемое облучением, восстанавливается более эффективно, если число хромосом больше, и что процесс восстановления не зависит от пола. Итак, снижение продолжительности жизни, вызванное радиацией, отличается от естественного старения. Здесь уместно процитировать Хендлера [42]: "Представление о том, что облучение приводит к преждевременному старению, верно наполовину и в широком смысле отражает нечеткость исходного параметра — продолжительности жизни".
Аналогичные наблюдения были проведены Томпсоном и Холлидеем [125] на уровне клеток in vitro. Когда фибробласты легких эмбриона человека (штамм MRC-5) обрабатывают колхицином в течение 3–6 ч, выживающая популяция содержит около 60 % тетраплоидных клеток, которые продолжают делиться. Продолжительность их жизни не отличается от продолжительности жизни диплоидных клеток. Сопоставима и скорость их роста. Если бы причиной смерти клеток было накопление мутаций или генетические дефекты, то тетраплоидные клетки должны были бы обладать большей устойчивостью и имели бы большую продолжительность жизни. Но это не так. Хён и др. [46] также наблюдали, что диплоидные фибробласты кожи человека имеют ту же продолжительность жизни, что и тетраплоидные. Если мутации и вносят свой вклад в процессе старения клеток в культуре, они не проявляют себя, в период активного роста (фаза II) и потому должны быть рецессивными. Возможно, что происходит постепенное увеличение генетического груза рецессивных дефектов, что может в итоге привести к инактивации одного или нескольких необходимых генов обеих гомологичных хромосом. Если это так, то тетраплоидные клетки могли бы противостоять большим повреждениям и имели бы большую жизнеспособность. Если мутации вредны, они вызывают гибель клеток и не аккумулируются. Диплоидные и тетраплоидные клетки, имели бы сходную продолжительность жизни только в том случае, если бы вредные мутации возникали в конце жизни.
Здесь уместно обсудить действие ионизирующей радиации на сперматогонии и виды животных с различной продолжительностью жизни. Сайнекс [114] сообщил, что приблизительная доза LD50 для сперматогониев, человека, мыши и дрозофилы составляет соответственно 50, 450, 500 и 6400 Р. Эти данные противоречат теории соматических мутаций, согласно которой клетки зародышевого пути устойчивы к мутациям, вызываемым ионизирующим излучением. Кроме того, в соответствии с этой теорией долгоживущие виды должны быть более устойчивыми к радиации, тем не менее человек, продолжительность жизни которого соответственно в 50 и 1200 раз больше, чем у мыши и дрозофилы, более чувствителен к радиации.
Уменьшение продолжительности жизни под влиянием облучения наблюдали у мыши [13, 14, 72], человека [110] и дрозофилы [3, 28, 69, 83]. Популяция дрозофилы, подвергнутая облучению дозой около 4500 рад, фактически живет дольше, чем контрольная [119]. Такой же результат получен на безмикробных мышах [127]. Симптомы, появляющиеся у облученных особей со сниженной продолжительностью жизни, отличаются от тех, которые возникают во время естественного старения без облучения. Следовательно, проникающая радиация не ускоряет процесс естественного старения, но вызывает раннюю смерть из-за повышения частоты рака или других болезней. Таким образом, укорочение жизни, вызванное ионизирующей радиацией, может представлять собой неспецифический эффект и быть следствием "радиационного синдрома", который не связан с естественным старением.
Главная трудность в оценке теории соматических мутаций состоит в отсутствии объективных способов измерения скорости накопления этих мутаций в постмитотических клетках. Единственный испробованный путь заключается в оценке смертности, которая может быть вызвана многими факторами. Кроме того, непонятно, почему клетки зародышевого пути более устойчивы к проникающей радиации. Увеличение продолжительности жизни у дрозофилы [119] и мыши [127] после воздействия излучения может быть побочным эффектом, хотя при больших дозах влияние излучения на смертность очевидно. Итак, накопление соматических мутаций не может быть причиной старения.
Следует рассмотреть другой тип изменений в хроматине, а именно повреждение структуры ДНК. Прайс и др. [94] изучали in vitro включение 3Н-тимидина в ДНК головного мозга, печени и сердца мышей различных возрастов при помощи радиоавтографии с использованием ДНК-полимеразы тимуса теленка. Более интенсивное включение наблюдали у старых мышей, что указывает на большую матричную активность ДНК. Авторы предположили, что это может быть вызвано появлением одноцепочных разрывов в ДНК, для ликвидации которых требуется дополнительный репаративный синтез. Кроме того, может иметь место утрата ферментов репарации, и тогда разрывы не восстанавливаются. Это согласуется с результатами Семиса и др. [109], которые обнаружили повышенное включение 3Н-тимидина в ДНК старых мышей. Наличие таких разрывов или повреждений ДНК в пожилом возрасте подтверждается сходными данными по чувствительности ДНК к нуклеазе S1, которая расщепляет одноцепочечные области. Четзанга и др. [16] показали, что ДНК печени старых 20-месячных мышей более чувствительна к нуклеазе S1, чем ДНК молодых (1-15 мес) мышей. Кроме того, было обнаружено, что в градиенте щелочной сахарозы ДНК головного мозга старых мышей осаждается полидисперсно в виде 4 зон, тогда как у молодых мышей осаждение монодисперсное — в виде одной зоны. Под действием нуклеазы S1 ДНК старых мышей распадается на большее число фракций с малой молекулярной массой. Предположение о деградации ДНК при старении строится также на основании данных о снижении транскрипции РНК хроматина печени в присутствии РНК-полимеразы [45].
Интенсивность внепланового репаративного синтеза ДНК в фибробластах после ультрафиолетового облучения была изучена Хартом и Сетлоу [43]. В фибробластах долгоживущих млекопитающих повреждения восстанавливались с большей скоростью, чем в фибробластах короткоживущих. Установлена линейная связь между логарифмом продолжительности жизни видов и интенсивностью включения 3Н-тимидина в их ДНК, т. е. большая продолжительность жизни может быть обусловлена более эффективной репарацией ДНК (рис. 9.3) [43]. Литтл [74] также сообщил, что репаративная способность ДНК снижена на поздних пассажах культивируемых фибробластов. Эти исследования, однако, не объясняют, почему репаративная активность ДНК снижается в пожилом возрасте или почему она больше у долгоживущих видов. Если это вызвано снижением уровня ферментов репарации, то необходимо знать причину этого снижения. Итак, имеется достаточно доказательств для утверждения, что старение не вызывается соматическими мутациями, возникающими в результате действия проникающей радиации и других экзогенных факторов.
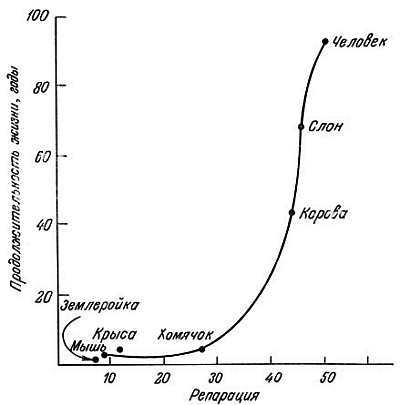
Рис. 9.3. Зависимость между продолжительностью жизни и интенсивностью включения нуклеотида, содержащего изотоп, в ДНК фибробластов в стандартных условиях в ходе репарации после ультрафиолетового облучения [43]