Альфа-связи в крахмале не только позволяют нам переваривать его, но и отвечают за другие важные свойства этого вещества. Цепи амилозы и амилопектина образуют спирали, а не плотно упакованные линейные структуры, как в целлюлозе. Молекулы воды, обладающие достаточной энергией, могут проникать внутрь спирали, поэтому крахмал растворим в воде, а целлюлоза – нет. Любой человек, имевший дело с крахмалом, знает, что его растворимость в воде зависит от температуры. Если нагреть суспензию крахмала в воде, его гранулы начинают впитывать больше воды, и при определенной температуре молекулы крахмала разделяются, образуя сеть распределенных в воде длинных нитей (так называемый гель). Мутная суспензия становится прозрачнее и гуще. Повара используют такие крахмалсодержащие вещества, как мука, тапиока и кукурузный крахмал, для придания соусам необходимой густоты.
В тканях животных сахара запасаются в виде гликогена, образующегося главным образом в клетках печени и скелетных мышц. Гликоген очень похож на амилопектин, но поперечные α-связи между атомами С1 и С6 встречаются в нем чаще – через каждые десять остатков глюкозы. В результате молекула получается сильно разветвленной. Для животных это чрезвычайно важно, и вот почему. У неразветвленной цепи только два конца, а разветвленная цепь, состоящая из того же количества остатков глюкозы, имеет гораздо больше концов. Когда нужно быстро получить энергию, можно одновременно отщеплять несколько остатков глюкозы от нескольких концов. Растениям, в отличие от животных, не приходится внезапно растрачивать энергию, убегая от хищников или преследуя добычу, так что хранение энергии в виде малоразветвленного амилопектина и неразветвленной амилозы вполне подходит для более медленных метаболических процессов в растениях. Это небольшое химическое различие, связанное лишь с числом, даже не с типом перекрестных сшивок, является основой одного из важнейших различий между растениями и животными.
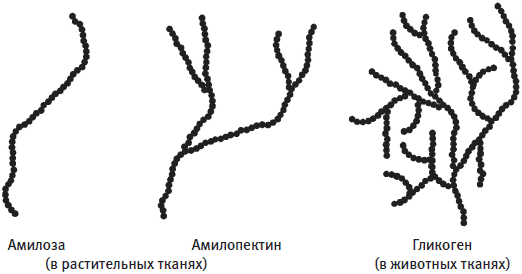
Характер ветвления полисахаридных цепей крахмала (амилоза и амилопектин) и гликогена. Чем сильнее разветвлен полимер, тем больше концов цепей доступно для фермента и тем быстрее высвобождается глюкоза.
Целлюлоза: настоящая бомба
В природе имеется большое количество запасных полисахаридов, однако структурного полисахарида (целлюлозы) существует гораздо больше. По некоторым оценкам примерно половина всего органического углерода на нашей планете содержится в составе целлюлозы. Ежегодно в природе синтезируется и расщепляется около 1014 кг целлюлозы (около ста миллиардов тонн). Целлюлоза уже давно привлекала внимание химиков и предпринимателей по той причине, что она является не только распространенным, но и восполняемым природным ресурсом.
К 30-х годам XIX века стало известно, что если целлюлозу растворить в концентрированной азотной кислоте, а образующийся раствор добавить в воду, получается легко воспламеняющийся взрывчатый белый порошок. Коммерческое использование этого вещества началось в 1845 году после открытий, сделанных в Базеле, в Швейцарии, немецким химиком Фридрихом Шенбейном. Он проводил эксперименты со смесями азотной и серной кислот дома, на кухне, чему активно противилась фрау Шенбейн, не желавшая, понятное дело, подвергать жилье опасности. Однажды, когда жены не было дома, Шенбейн пролил немного смеси кислот. Чтобы вытереть жидкость, он схватил первое, что попалось под руку – хлопчатобумажный фартук жены. Химик вытер кислоту и повесил фартук над печкой, чтобы высушить. Однако фартук взорвался, произведя страшный грохот и породив столб пламени. Неизвестно, что сказала жена ученого, когда вернулась домой и застала мужа за продолжением кухонных экспериментов с хлопком и азотной кислотой. Мы знаем только, что Шенбейн назвал новое вещество Schieβbaumwolle, “стреляющий хлопок”. Хлопок на 90 % состоит из целлюлозы, и теперь мы знаем, что “стреляющий хлопок” Шенбейна был нитроцеллюлозой (пироксилином), образующейся при замене атомов водорода в некоторых OH-группах в молекуле целлюлозы на нитрогруппы (NO2). Чем больше таких замен, тем взрывоопаснее вещество.
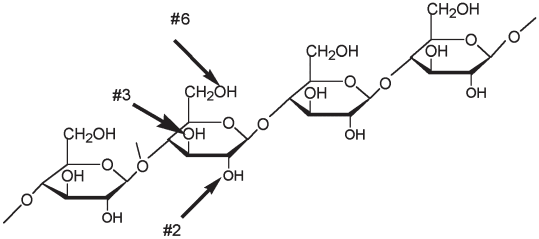
Участок молекулы целлюлозы с указанием мест возможного нитрования OH-групп у атомов С2, С3 или С6 в любом остатке глюкозы
Участок молекулы нитроцеллюлозы: в данном случае атомы водорода из OH-групп заменены нитрогруппами во всех возможных положениях в каждом остатке глюкозы
Шенбейн, осознавший возможную выгоду от своего открытия, основал фабрики по производству нитроцеллюлозы, надеясь, что она сможет заменить порох. Однако нитроцеллюлоза – очень опасное вещество, которое необходимо беречь от влаги. В те времена не знали, что азотная кислота является чрезвычайно едким веществом, и на нескольких фабриках произошли сильные взрывы, что вынудило Шенбейна закрыть производство. Только в конце 60-х годов XIX века, когда был разработан метод очистки нитроцеллюлозы от остатков азотной кислоты, стало можно получать достаточно устойчивую нитроцеллюлозу для промышленного производства взрывчатки.
Позднее был разработан контролируемый процесс, позволяющий получать разную нитроцеллюлозу: пироксилин с высоким содержанием нитрогрупп и такие вещества, как коллодий и целлулоид, отличающиеся низким содержанием нитрогрупп. Коллодий – это нитроцеллюлоза, смешанная со спиртом и водой. Эту смесь использовали на заре развития фотографии. Целлулоид (смесь нитроцеллюлозы с камфарой) – одна из первых пластмасс, из которой делали первую кинопленку. Другое производное целлюлозы – ацетат целлюлозы – оказалось гораздо менее горючим, чем нитроцеллюлоза, и быстро заменило ее во многих областях. Современные фото– и кинопроизводство обязаны своим нынешним размахом многогранной структуре целлюлозы.
Целлюлоза не растворима в большинстве растворителей, но переходит в щелочной раствор одного органического вещества – сероуглерода. В результате образуется ксантат целлюлозы. Эту вязкую дисперсию назвали вискозой. Если вискозу продавить через мелкие отверстия, а потом обработать кислотой, целлюлоза опять принимает форму тонких волокон, которые можно прясть. Так получают вискозный шелк. В похожем процессе, в котором вискозу продавливают через узкую щель, получают целлофан. Вискозу и целлофан обычно относят к синтетическим материалам, однако их нельзя считать полностью синтетическими: они созданы на основе природной целлюлозы.
И α-полимер глюкозы (крахмал), и β-полимер (целлюлоза) остаются важным компонентом нашего питания и продолжают оказывать влияние на нашу жизнь. Однако историческая роль целлюлозы и ее производных не связана с их пищевой функцией. Целлюлоза в форме хлопка явилась причиной двух важнейших событий XIX века: Промышленной революции в Европе и Гражданской войны в США. Хлопок послужил “топливом” Промышленной революции, изменившей развитие Англии и сопровождавшейся переселением сельских жителей в города, быстрой индустриализацией, инновациями, социальными изменениями и, наконец, процветанием страны. С другой стороны, с хлопком связан один из самых серьезных кризисов в истории Америки, поскольку одной из главных причин Гражданской войны были разногласия по вопросу о рабстве между свободным Севером и рабовладельческим Югом, экономика которого была основана на труде невольников, работавших на хлопковых плантациях.
Нитроцеллюлоза (пироксилин) – одно из первых взрывчатых веществ, созданных человеком, и ее открытие послужило толчком к развитию многих отраслей современной промышленности, поначалу связанных с различными формами нитроцеллюлозы (производство взрывчатых веществ, фото– и киноиндустрия). Производство синтетических тканей, начавшееся с вискозы, в XX веке сыграло важную роль в развитии экономики. Без целлюлозы наш мир был бы совсем другим.