Окруженные потенциальными фаговыми захватчиками, бактерии развили множество защитных систем, чтобы отслеживать и уничтожать эту угрозу. Когда я изучал биохимию в 1980-х гг., нам рассказывали, что бактерии обладают целой армией нуклеаз – высокоактивных ферментов, которые распознают и атакуют определенные мотивы чужеродной ДНК. (Последовательности ДНК самих бактерий защищены от этих нуклеаз химическими метками, подобно тому как розетки закрыты от детей специальными крышками). Ученые использовали эти ферменты ограничения как средство для разрезания, обмена или «сшивания» (лигирования) фрагментов ДНК, например помещая гены человека в ДНК бактерии, что положило начало развитию отрасли биотехнологии. Но, как мы убедимся далее, теперь мы знаем, что бактерии обладают еще и другой иммунной системой. CRISPR – это небольшой участок бактериального генома, который содержит фрагменты захваченного вирусного генома для дальнейшего использования, причем каждый такой фрагмент (или спейсер) отделен от другого одинаковыми повторяющимися палиндромными последовательностями ДНК. Представьте себе это как картотеку ФБР, в которой хранятся данные о разыскиваемых преступниках.
CRISPR – это больше, чем просто хранилище вирусных злодеяний. Совсем рядом находится арсенал мощной системы противоракетной обороны «земля – воздух». Когда клетка обнаруживает вторгшийся вирус, первым делом активируется система CRISPR, производящая копии РНК заархивированных вирусных последовательностей. Эта цепочка РНК затем разрезается на отдельные фрагменты, каждый из которых соответствует тому или иному вирусу и служит в качестве наброска внешности возможного преступника, сделанного полицейским художником. Сама по себе РНК не может причинить никакого вреда, поэтому она превращается в оружие путем связывания с ферментом, расщепляющим ДНК, называемым Cas (от англ. CRISPR-associated sequence – «последовательность, связанная с CRISPR»), образуя рибонуклеопротеиновый комплекс, оснащенный сигналом GPS и готовый к бою.
В микроскопической вселенной существует полдюжины разновидностей или типов систем CRISPR, которые делятся на два класса в зависимости от их строения и свойств[68]. Одна из простейших структур – тип II – содержит фермент Cas9. Эта нуклеаза, подобно кусачкам для проводов, добивается полноценного разрыва обеих цепей ДНК, но делает это избирательно. Она захватывает крРНК и держит ее как фотоснимок преступника – и ищет совпадения в вирусной ДНК. При обнаружении необходимого участка Cas9 и крРНК «защелкиваются» на ДНК и разрезают ее, нейтрализуя угрозу. «Cas9 поистине творит чудеса, – объясняет Урнов. – Когда она охраняет внутриклеточное пространство от вторжений, она буквально носит с собой копию объявления о разыскиваемом преступнике, спрашивая каждого: "Извините, ведь вы – точная копия разыскиваемого преступника, не правда ли? Тогда я вас порежу"»[69].
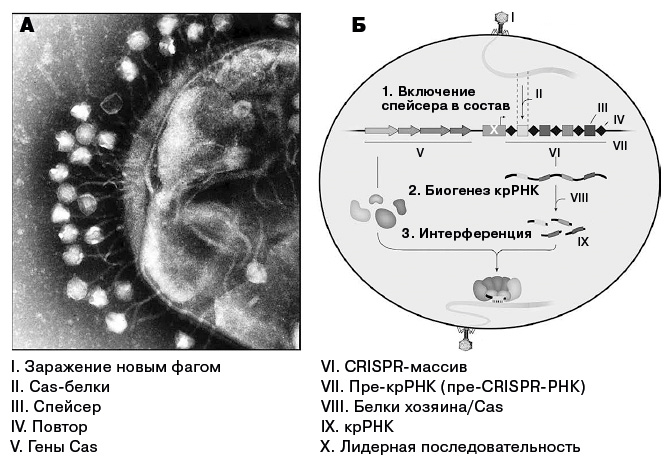
Фаги и каскад реакций CRISPR. (А) Замечен в момент совершения преступления: фаги садятся на поверхность клетки E. coli (кишечной палочки), чтобы совершить нападение. (Б) CRISPR-Cas-иммунитет. 1. Бактерия захватывает фрагменты вирусной ДНК и включает эти фрагменты как спейсеры в расширяющийся блок последовательностей CRISPR. 2. Для борьбы с фаговой инфекцией массив CRISPR транскрибируется в РНК, которая называется (пре-крРНК), а затем преобразуется в зрелые крРНК. 3. На стадии противодействия крРНК и Cas белок(и) образуют комплекс, который разрушает распознанные фаговые последовательности. Некоторые системы CRISPR (класс 1) содержат несколько белков Cas (как показано на рисунке), в то время как более простой системе класса 2 требуется одна нуклеаза – Cas9 (по материалам пункта 15 примечаний)
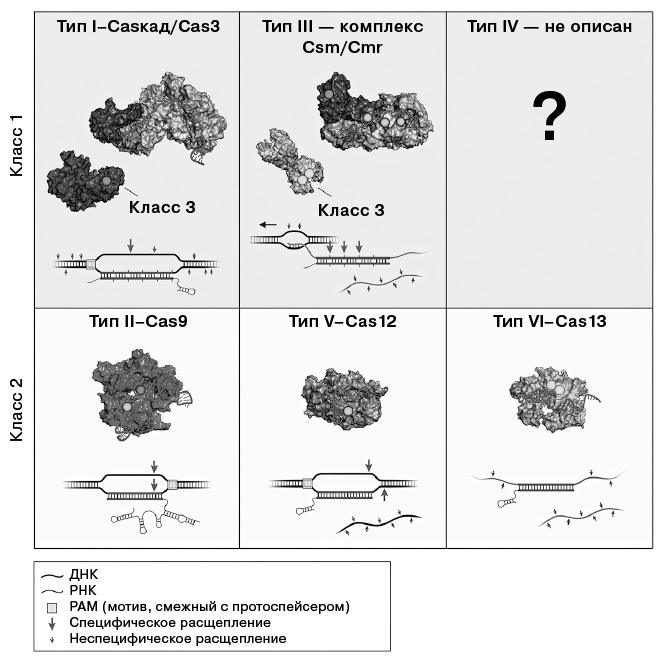
Описанные системы CRISPR. Существует несколько разновидностей систем CRISPR, которые делятся на два класса – класс 1 и класс 2. В классе 1 расщепление ДНК осуществляется комплексом белков, иногда называемых каскадом от слова Cas. В классе 2 системы CRISPR содержат одну нуклеазу Cas, такую как Cas9, Cas12 или Cas13. (Подробнее см. пункт 15 примечаний.)
Марраффини показывает, как две бактериальные системы защиты дополняют друг друга. Рестриктазы создают первый барьер защиты от вирусной угрозы, дробя вирусную ДНК на части, которые могут быть включены в массив CRISPR. Однако, если фаги, когда-либо эволюционировавшие, уклоняются от первой линии защиты, срабатывает иммунизация CRISPR. «Это аналогично вакцинации, – говорит Марраффини. – Когда ДНК фагов мертва, CRISPR может собрать спейсеры для формирования иммунитета у бактерии». Лишь немногие инфицированные вирусом бактерии действительно приобретают спейсеры – примерно 1 на 1 млн, но это дает одной клетке возможность устранить вирусную угрозу и восстановить популяцию[70].
В документальном фильме Адама Болта «Природа человека» (Human Nature, 2019) мы знакомимся с Дэвидом Санчесом, очаровательным мальчиком, страдающим от серповидноклеточной анемии. Узнав о возможностях CRISPR в лечении его болезни, он проницательно спрашивает: «Как эта штука работает и откуда она знает, как воздействовать на нужный ген, а не на тот, что отвечает за рост волос?»
Гениальность революции CRISPR заключалась в том, чтобы привязать Cas9 не к вирусной РНК, как в природе, а к синтетически разработанной РНК, запрограммированной исследователями, которая позволяет им воздействовать практически на любую последовательность ДНК любого гена любого организма. В результате у нас в руках оказался бактериальный фермент, существующий миллиард лет, и мы перепрофилировали его в молекулярный скальпель точной генной хирургии XXI в. Независимо от того, чей геном мы хотим отредактировать: хомяка или человека, комара или мыши, красной смородины или красного дерева, – процесс остается по сути одним и тем же. Это связано с тем, что все организмы в природе используют один и тот же универсальный код ДНК, состоящий из одного и того же четырехбуквенного алфавита.
В своем естественном состоянии Cas9 не интересуется ДНК, в основном случайно сталкиваясь и отскакивая от нее. Но как только Cas9, имеющая форму ладони, захватывает направляющую РНК, точная реконфигурация структуры белка заставляет ее взаимодействовать с ДНК в поисках подходящей мишени. По словам Блейка Виденхефта, профессора Университета штата Монтана, белковые комплексы Cas «патрулируют все внутриклеточное пространство, находят чужеродную [вирусную] ДНК, связываются с ней и приговаривают ее к уничтожению в считаные минуты… это довольно впечатляющий процесс»[71].
Поиск и связывание с целевой последовательностью происходят в два этапа. Прежде всего Cas9 ищет короткий мотив ДНК, называемый последовательностью PAM[72], – маяк, который дает ферменту сигнал для кратковременного связывания с ДНК, и взаимодействует с ним. «Это мимолетное взаимодействие приводит к искривлению ДНК», – объясняет Виденхефт. Изгибая ДНК, Cas9 расцепляет нити двойной спирали, чтобы направляющая РНК могла проскользнуть в образовавшуюся щель (создавая так называемую R-петлю)[73]. Направляющая РНК быстро сверяет последовательность с текстом целевой ДНК. Если будет найдено идеальное совпадение среди всех двадцати оснований (букв текста), то ДНК-последовательность будет уничтожена. Cas9 рассекает[74] обе нити ДНК так же ровно, как кухонный нож, создавая двухцепочечный разрыв (DSB, double-strand break) всего в нескольких основаниях от последовательности PAM[75].