Рис. 1.6. Процесс структурирования воды в поле Li+.
В водном растворе в результате этого литий имеет наибольший радиус, что объясняет его меньшую подвижностьпо сравнению с подвижностью ионов калия и натрия. По величине гидратированного иона лития (10 Å) можно вычислить, что в первой сфере он имеет – 6, во второй – 30, а в третьей – 76 молекул воды, что естественно, оказывает определяющее влияние на его химические свойства и физико-химическое поведение в водных растворах.
Внешнесферные комплексы могут быть идентифицированы по изменению некоторых характеристик, в частности, спектральных. Для лабильных систем (когда лиганды, входящие в состав внутренней и внешней сфер, могут легко меняться местами) трудно провести различие между внешнесферными и внутрисферными комплексами. Возможно, превращение внешнесферного комплекса во внутрисферный происходит в результате химической реакции
скорость которой определяется скоростью образования ионной пары и, в дальнейшем, внутрисферного комплекса. Возможность перехода одной формы комплекса в другую характеризует лабильность комплекса. Оказывается, что комплексы трехвалентных РЗЭ чрезвычайно лабильны. Причина этого, по-видимому, в большом координационном числе ионов РЗЭ. Скорость определяющей реакцией будет удаление молекулы воды из внутренней координационной сферы и ее замещение на лиганды второй внешней координационной сферы.
Устойчивость комплексных соединений
Обычно реакции комплексообразования рассматривают, используя понятия теории кислот и оснований Льюиса.
Характерные свойства кислот и оснований можно связать с их электронной структурой, а в особенности с парой электронов, образующих координационную ковалентную связь. Тогда можно дать следующее определение:
кислоты – вещества, которые при образовании ковалентной связи принимают пару электронов (являются акцепторами пары электронов);
основания – вещества, которые при образовании ковалентной связи отдают пару электронов (являются донорами пары электронов). Выбор электронной конфигурации в качестве фундаментального критерия для обоснования понятий «кислота» и «основание» дает возможность применить их для более широкого класса веществ.
Основания – это соединения, обладающие неподеленной парой электронов, которая может быть использована для образования устойчивой электронной группировки другого атома; кислота – соединения, которые могут использовать неподеленную пару электронов атома другой молекулы с тем, чтобы завершить образование устойчивой электронной конфигурации одного из своих собственных атомов. Развитием электронной теории кислот и оснований является концепция «жестких» и «мягких» кислот и оснований Пирсона (1963 г.). В предложенной теории в качестве основного процесса кислотно-основного равновесия рассматривается взаимодействие акцептора пары электронов А (кислоты) с донором пары электронов В (основанием) с образованием стабильного кислотно-основного комплекса АВ:
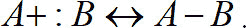
Однако, в то время как Льюис считал самым важным при образовании комплекса появление ковалентной связи, Пирсон включил в рассмотрение и другие типы взаимодействия, в том числе и те, которые приводят частично или полностью к электростатической (ионной) связи. Таким образом, к кислотно-основным реакциям, например, относятся реакции образования комплексных катионов и анионов, а также формирование кристаллической решетки солей. Вопрос состоит в том, какие свойства кислоты А и основания В обеспечивают термодинамическую стабильность образования комплекса АВ. Теория предполагает, что в качественном отношении эта стабильность определяется так называемой жесткостью и мягкостью участников реакции.
Если, например, рассматривать комплексообразование с галогенидами, то для различных катионов будет наблюдаться различная закономерность устойчивости образующихся комплексов. Первые константы образования уменьшаются в следующей последовательности:
Таким же образом можно классифицировать не только комплексообразователи, но и лиганды. Отличие надо искать в свойствах их электронной структуры и реакционной способности.
Жесткие частицы обладают прочной малодеформируемой электронной структурой. Это могут быть атомы элементов с высокой электроотрицательностью (F, O, N) или катионы с большим зарядом. Напротив, мягкие частицы имеют подвижную деформируемую электронную структуру и высокую поляризуемость.
Жесткие кислоты. Электронная оболочка жестких кислот характеризуется высокой стабильностью относительно внешних электрических полей. Наиболее жесткой кислотой является протил, который из-за отсутствия электронной оболочки и чрезвычайно малого радиуса прочно связывается с активным центром молекулы основания. Следовательно, характеризуется наименьшим размером, во внешней сфере нет неподеленной пары электронов. Типичные представители жестких кислот имеют структуру инертного газа Li+, Be2+, Al3+… и относятся, в основном, к элементам главных подгрупп периодической системы. К последним близки по свойствам некоторые катионы переходных металлов с не полностью занятой d-оболочкой (Mn2+, Fe3+…).
Жесткие основания вследствие прочной и устойчивой электронной оболочки, а также соответствующего строения электронных орбиталей не имеют склонности к образованию ковалентных связей с катионом (F-, O2-). Рассматривая реакционную способность воды, как донора пары электронов. Можно отметить, что, например, при гидратации катионов, кислород молекулы вода как раз и является жестким центром. Анионы кислородсодержащих кислот, таких как ClO4-, SO42-, PO43-, CO32- также имеют малодеформируемую структуру.
В противоположность, мягкие кислоты – большие катионы с деформируемой электронной оболочкой (например, элементы главных подгрупп Cs+, Tl+) а также катионы переходных металлов, в электронной оболочке которых имеются неподеленные пары электронов. Способность к поляризуемости у них выше. Мягкость соединений увеличивается по мере уменьшения положительного заряда ионов.
Аналогично и мягкие основания (P3-, S2-, I-, Br-), способность к поляризуемости у которых высока.
Анализируя константы устойчивости комплексов, можно сделать вывод, что жесткие кислоты образуют наиболее прочные соединения с жесткими основаниями, а мягкие кислоты – с мягкими основаниями. Большое значение имеет и то, каким образом формируется соответствующее соединение, что определяет молекулярный контакт при образовании этого соединения:
Таким образом, можно провести классификацию комплексообразователей и лигандов (табл.1.2).
Таблица 1.2.
Распределение кислот и оснований по Пирсону.
Актиноиды – типичные жесткие кислоты, для них выполняется следующая зависимость: М4+ > M3+ > MO22+ > МO2+. Жесткие кислоты, взаимодействуя с жесткими основаниями, образуют соединения, прочность которых подчиняется величине ионного потенциала.