Приближение Борна-Оппенгеймера
Очень хороший способ понять, как связываются атомы водорода, когда они сближаются и образуют молекулу водорода, основывается на концепции, известной как приближение Борна-Оппенгеймера. Как говорилось в главе 5, Борн получил Нобелевскую премию по физике в 1954 году за свою вероятностную интерпретацию волновой функции. Оппенгеймер внёс большой вклад в физику. Наибольшую известность он получил как физик, руководивший во время Второй мировой войны Манхэттенским проектом, в рамках которого разрабатывалась и испытывалась первая атомная бомба. В приближение Борна-Оппенгеймера требуется поместить два ядра атомов водорода (два протона) на фиксированном расстоянии друг от друга. Начнём с расстояния, которое вы сочтёте достаточно большим, чтобы атомы водорода не чувствовали друг друга. Выполним квантовомеханический расчёт энергии. Если атомы находятся далеко друг от друга, то эта энергия будет равна просто удвоенной энергии атома водорода в 1s-состоянии, поскольку имеется всего два атома водорода. Теперь немного уменьшим расстояние и повторим вычисления, а потом ещё уменьшим расстояние и вновь выполним вычисления. Когда расстояние между ядрами в нашем расчёте станет достаточно малым, атомы почувствуют друг друга. Если должна образоваться химическая связь, то есть если два атома водорода собираются объединиться в молекулу водорода, то энергия должна убывать. Для образования связи энергия молекулы должна быть меньше, чем энергия атомов, когда они разнесены далеко друг от друга.
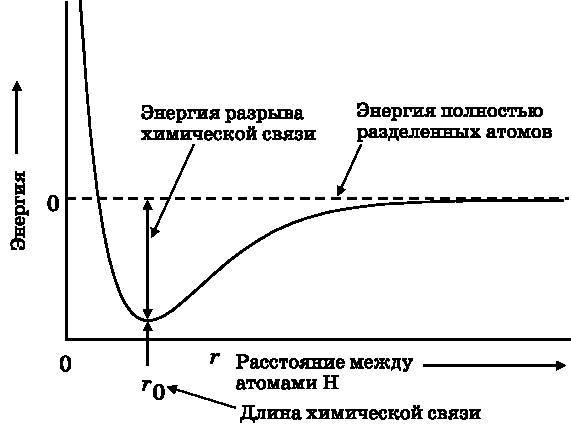
Рис. 12.1. График зависимости энергии двух атомов водорода от расстояния между ними. Когда два атома H находятся очень далеко друг от друга, энергия системы равна сумме энергий 1s-орбиталей двух атомов H. Эта величина принимается за нулевое значение энергии, отмеченное штриховой линией. При сближении атомов энергия убывает, пока не достигает минимума. Если атомы сближаются ещё сильнее, энергия быстро возрастает
На рис. 12.1 представлен график изменения энергии двух атомов водорода в процессе их сближения друг с другом. Как уже отмечалось, когда два атома водорода находятся очень далеко друг от друга, они не взаимодействуют. Каждый из них имеет энергию, соответствующую 1s-орбитали атома водорода. Будем считать это нулевым уровнем энергии. Сам по себе атом водорода имеет отрицательную энергию, как это объяснялось в главе 10. Эта энергия соответствует энергии связи электрона с протоном (ядром). Сейчас нас интересует изменение энергии, когда два атома водорода вступают во взаимодействие. Мы хотим найти энергию, ассоциированную с химической связью, поэтому нулевая энергия — это та, при которой химическая связь отсутствует. На рис. 12.1 нулевая энергия обозначена штриховой линией. Это энергия, соответствующая состоянию, когда атомы полностью разделены. По горизонтальной оси отложено расстояние r между двумя атомами H. По мере сближения атомов H энергия начинает убывать, причём всё быстрее и быстрее. Она достигает минимума при расстоянии между атомами r0 (см. рис. 12.1). Если атомы сближаются ещё сильнее, энергия очень быстро возрастает, то есть когда атомы находятся слишком близко, они отталкиваются друг от друга. Поскольку при сближении двух атомов энергия убывает, между ними образуется химическая связь.
Длина химической связи — это расстояние, которое обеспечивает наименьшую энергию
На расстоянии r0 энергия достигает минимума. Это расстояние между атомами H является наиболее устойчивым (обладает наименьшей энергией). Оно называется длиной химической связи. Это расстояние между двумя протонами в устойчивой молекуле водорода. Разность между дном энергетической «потенциальной ямы» и нулевой энергией составляет энергию разрыва химической связи (энергию диссоциации). Она равна количеству энергии, которую надо передать молекуле водорода, чтобы разорвать химическую связь и получить два отдельных атома водорода. Потенциальная яма для молекулы водорода подобна яме в земле, в которую скатывается мяч. Вне ямы энергия равна нулю. Мяч падает на дно ямы, чтобы минимизировать гравитационную потенциальную энергию. Гравитация тянет мяч вниз. Чтобы поднять мяч из потенциальной ямы, требуется энергия, поскольку нужно преодолеть гравитационное притяжение, действующее на мяч. Чем глубже яма, тем больше энергии потребуется, чтобы поднять из неё мяч. В случае с молекулами чем глубже потенциальная яма, тем больше энергии нужно, чтобы из неё выбраться, то есть разорвать химическую связь.
На рис. 12.1 не показана шкала расстояний по оси r. Интересно, однако, рассмотреть два расстояния. На какой дистанции атомы водорода впервые начинают ощущать присутствие друг друга? На рис. 10.3 видно, что волна амплитуды вероятности для 1s-орбитали атома водорода становится очень малой на расстоянии от ядра около 3 Å (3∙10−10 м). Так что можно ожидать, что два атома водорода начнут взаимодействовать, если сойдутся чуть ближе 6 Å. На рис. 12.1 точка, где кривая потенциальной энергии (сплошная линия) начинает отклоняться от линии нулевой энергии (штриховая прямая), находится примерно на 6 Å, так что атомы начинают чувствовать друг друга, как только у их атомных волновых функций возникает существенное перекрытие. Точка r0 — это положение минимума на кривой потенциальной энергии. Она соответствует длине химической связи. Эксперименты и расчёты показали, что это расстояние составляет 0,74 Å. Если расстояние между атомами больше или меньше этого значения, энергия будет выше.
Кривая потенциальной энергии, изображённая на рис. 12.1, получена на основе реальных квантовомеханических расчётов. Это относительно несложные вычисления, которые можно целиком выполнить с помощью карандаша и бумаги, компьютеры для этого не нужны. По результатам приближённых вычислений r0=0,80 Å, так что они не вполне точны. Если хотите увидеть огромный объём математических выкладок, которые требуются даже для этого относительно простого расчёта, загляните в главу 17 моего учебника основ квантовой механики (Michael D. Fayer. Elements of Quantum Mechanics. New York: Oxford University Press, 2001). Намного более сложные квантовые теоретические вычисления для молекулы H2 позволяют получить все свойства молекулы водорода с точностью выше достижимой в экспериментальных измерениях. Точные вычисления возможны благодаря тому, что молекула водорода очень проста. Для крупных молекул эксперименты всё ещё превосходят вычисления по точности.
Образование связывающих молекулярных орбиталей
Из рис. 12.1 видно, что между двумя атомами водорода будет формироваться химическая связь, в результате чего образуются молекулы H2, но неясно, каким образом. Как отмечалось в главе 11, ковалентная связь состоит в том, что атомы совместно используют электроны. Когда образуется молекула, атомные орбитали объединяются и формируют молекулярные орбитали. Для молекулы водорода мы начнём с двух атомов водорода: Ha и Hb. Каждый из них имеет один электрон атомной 1s-орбитали. Обозначим эти орбитали 1sa и 1sb. В верхней части рис. 12.2 они показаны кружками. Это простое схематическое изображение делокализованной волны амплитуды вероятности электрона, представленной на рис. 10.2-10.4. В нижней части рисунка показано, что происходит, когда два атома сближаются так, что расстояние между ними становится равным длине химической связи r0 (см. рис. 12.1). Волновые функции имеют знак. В данном случае их знаки положительные.