Рис. 39. Схема рестриктазно-лигазного метода
Однако после такого спаривания полной целостности двойной спирали не восстановится, поскольку останется два разрыва в фосфодиэфирном остове. Для его восстановления, то есть сшивания, или лигирования нитей используют фермент ДНК-лигазу. Этот фермент в живой клетке выполняет ту же функцию — сшивание фрагментов ДНК, синтезирующихся при репликации.
Сшивка по "тупым" концам (коннекторный метод)
Липкие концы не абсолютно необходимы для связывания фрагментов ДНК. Тупые концы также могут быть соединены за счет действия ДНК-лигазы, если и лигаза, и тупые концы присутствуют в реакционной смеси в высоких концентрациях. В этом случае реакция лигирования имеет свои особенности и ее эффективность ниже, чем при сшивке по липким концам. Впервые такие эксперименты были выполнены в 1972 году Полем Бергом в Стенфордском университете, США. Липкие концы также можно ферментативным путем присоединить к молекулам ДНК с тупыми концами. Для этого используют фермент — концевую трансферазу из тимуса теленка, которая присоединяет нуклеотиды к 3-концам цепей ДНК. Если к 3'-концам одного из рекомбинируемых in vitro фрагментов ДНК с помощью концевой дезоксинуклеотидилтрансферазы достроить одноцепочечные олиго (dA) — сегменты определенной длины, а к концам другого фрагмента — олиго (dT) — сегменты примерно такой же длины, то при смешении полученных таким образом фрагментов происходит спаривание за счет образования водородных связей между олиго (dA) — и олиго (dT) — последовательностями (рис. 40). Для ковалентного соединения двух фрагментов используется ДНК-лигаза. Эти процедуры составляют основу для второго общего метода получения рекомбинантных молекул ДНК.
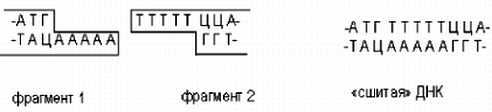
Рис. 40. Пришивание «липких» концов и сшивка фрагментов ДНК
Поскольку можно формировать достаточно длинные взаимокомплементарные одноцепочечные концы, гибридные молекулы образуются с высокой эффективностью. В частности, поэтому при клонировании ДНК-копий матричных РНК, которые доступны в ограниченных количествах, обычно используют коннекторный метод. При таком способе соединения между фрагментами встраиваются участки ААААА. Такие дополнительные последовательности ТТТТТ могут влиять на функции соединяемых молекул и поэтому всегда, когда только возможно, для получения рекомбинантных молекул ДНК пользуются липкими концами, образовавшимися в результате действия рестриктаз.
Сшивка фрагментов с разноименными липкими концами
В ситуации, когда необходимо сшить фрагменты, образованные разными эндонуклеазами рестрикции, и имеющие разные, то есть некомплементарные друг другу липкие концы, применяют так называемые линкеры (или "переходники"). Линкеры — это химически синтезированные олигонуклеотиды, представляющие собой сайты рестрикции или их комбинацию. Впервые эту идею предложил Шеллер с сотрудниками в 1977 году.
Существуют большие наборы таких генных "переходников". Естественно, что при использовании линкеров должна учитываться необходимость соблюдения правил экспрессии генетической информации. Часто в середину линкера помещают какой-либо регуляторный генетический элемент, например, промотор или участок, связанный с рибосомой. В этом случае линкеры обеспечивают не только объединение генов, но и обуславливают их экспрессию. Существуют линкеры "тупой конец — липкий конец".
При необходимости липкие концы можно превратить в тупые. Это достигается либо отщеплением липких концов с помощью фермента — эндонуклеазы S1, которая разрушает только одноцепочечную ДНК, либо липкие концы "застраивают", то есть с помощью ДНК-полимеразы I на однонитевых липких концах синтезируют вторую нить.
ОПРЕДЕЛЕНИЕ НУКЛЕОТИДНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ (СЕКВЕНИРОВАНИЕ) ДНК
Описанные методы, позволившие идентифицировать генетически важные участки ДНК, имели большое значение сами по себе. Но они также проложили путь к разработке исключительно эффективных методов секвенирования ДНК и создания рекомбинантных молекул. Секвенирование позволяет довольно быстро определить полную нуклеотидную последовательность сегмента длиной 100–500 нуклеотидных пар, образующегося при расщеплении ДНК рестрикционными эндонуклеазами.
Метод Маскама и Гилберта (химический)
Один из методов основан на химической деградации ДНК. Он был предложен в 1976 году Максамом и Гилбертом и назван их именем. Суть метода сводится к следующему: один из концов фрагмента ДНК метят с помощью изотопа фосфора 32Р. В последнее время вместо радиоактивной вводят флюоресцирующую метку. Ее можно «цеплять» и к нуклеотидам, причем для каждого типа нуклеотидов подбирать различную окраску. Препарат меченой ДНК делят на четыре порции и каждую из них обрабатывают реагентом, специфически разрушающим одно или два из четырех оснований, причем условия реакции подбирают таким образом, чтобы на каждую молекулу ДНК приходилось лишь несколько повреждений.
Разрушение идет в 2 этапа. На первом этапе происходит модификация азотистого основания и последующее выщепление его. На втором этапе производят гидролиз ДНК в местах выщепления оснований. Пуриновые основания модифицируются диметилсульфатом. Адениновые остатки метилируются по третьему атому азота, гуаниновые — по положению N7. Если такую модификацию обработать 0,1 М НСl при 0 °C, то выщепляется метиладенин. При последующей инкубации в щелочной среде (0,1 М NaOH) при температуре +90 °C происходит разрушение сахаро-фосфатной связи в местах выщепления оснований. Обработка поврежденных молекул пиперидином приводит к гидролизу ДНК по остаткам метилгуанина. Пиримидиновые основания модифицируются гидразином. В бессолевой среде модифицируется и цитозин, и тимин, в присутствии 2 М NaCl модифицируется только цитозин. При дальнейшей обработке пиперидином происходит расщепление ДНК по точкам модификации. Можно использовать и другие реакции химической модификации оснований и расщепления по ним молекул ДНК. В результате получается набор меченых фрагментов, длины которых определяются расстоянием от разрушенного основания до конца молекулы. Фрагменты, образовавшиеся во всех четырех реакциях, подвергают электрофорезу в четырех соседних дорожках; затем проводят радиоавтографию, и те фрагменты, которые содержат радиоактивную метку, оставляют "отпечатки" на рентгеновской пленке. По положению отпечатков можно определить, на каком расстоянии от меченого конца находилось разрушенное основание, а зная это основание — его положение. Так набор полос на рентгеновской пленке определяет нуклеотидную последовательность ДНК. Аналогично наблюдают флюоресцентное окрашивание. Если для каждого из четырех нуклеотидов был подобран свой цвет флюоресцентной метки, то при электрофорезе их наносят на 1 дорожку. Тогда расположение нуклеотидов отмечено штрихами разного цвета, а процедуру считывания легко автоматизировать.
Метод Сэнгера (ферментативный)
Другой метод, разработанный Сэнгером и носящий его имя, основан не на химическом, а на ферментативном подходе. Сэнгер использовал ДНК-полимеразу I. В клетке этот фермент участвует в процессе репликации, заполняя пробелы между вновь синтезированными фрагментами ДНК (фрагментами Оказаки). Для работы фермента в пробирке требуются предшественники ДНК — дезоксирибонуклеотидтрифосфаты (dNTP), а также одноцепочечная матрица, на которой должен быть небольшой двухцепочечный участок — затравка, с которого начинается синтез (рис. 41). Были также синтезированы модифицированные дидезоксирибонуклеотиды, в которых дезоксирибоза 3'-ОН отсутствует, для каждого из четырех оснований ДНК. ДНК-полимераза включает эти предшественники в ДНК. Однако, включившись в ДНК, модифицированное основание не может образовать фосфодиэфирную связь со следующим дезоксирибонуклеотидом. В результате рост (элонгация) данной цепи останавливается (терминируется) в том месте, где в ДНК включился дидезоксирибонуклеотид (ddNTP). Поэтому их называют терминаторами элонгации.