Неестественность двумерных клеточных формирований стала очевидной больше века назад, и почти с тех же пор ее пытались преодолеть. Упомянутый в прошлой главе Росс Гаррисон в 1906 году сообщил, что вырастил нервные волокна в свернувшейся капле лимфы, поместив в нее фрагмент ткани лягушачьего эмбриона. В последующие десятилетия ряд исследовательских групп показал, что эмбрионы разных биологических видов можно разделять на клетки, которые, получив свободу в трех измерениях, способны собираться в агрегаты, воспроизводящие некоторые черты нормального зародыша7.
Со временем ученые поняли, что для функционирования клеток критически важна белково-углеводная сетчатая структура за их пределами – внеклеточный матрикс: он не только служит каркасом для органов и тканей, но и поставляет механические и химические сигналы, управляющие экспрессией генов и даже клеточными судьбами. В 1980-х, например, группа Мины Бисселл из Национальной лаборатории им. Лоуренса в Беркли (Калифорния) вырастила ткани молочной железы, способные выделять молоко под контролем соответствующего матрикса, наглядно этим показав, что полученные кластеры клеток не только выглядели, но и работали как положено. С помощью растущего арсенала методов трехмерного культивирования ученые затем начали выращивать и другие ткани, включая опухолевые. Эта отрасль получила сильный импульс к развитию в XXI веке, когда наши представления об основополагающих механизмах онтогенеза дополнились представлением об идеальных «семенах» для выращивания тканей – стволовых клетках.
Комбинируя техники манипуляций со стволовыми клетками и методы трехмерного культивирования, мы получаем поразительное разнообразие работоспособных самоорганизующихся клеточных ансамблей практически любого типа, по замыслу приближающихся к тем самым «органам в чане». Такие ансамбли называют органоидами вне зависимости от того, происходят они от стволовой клетки или нет8. Клетки, которые отшелушиваются со стенки вашего кишечника, заменяются потомками стволовых клеток, залегающих на дне миллиардов эпителиальных углублений, или крипт. В 2009 году группа Ханса Клеверса из нидерландского Утрехта показала, что единственная стволовая клетка кишечника, должным образом выращенная в трехмерном матриксе, может породить целое клеточное сообщество в форме неровного шара с четко определяемым внутренним пространством, ограниченным теми же типами клеточных поверхностей, что и реальный просвет кишки9; на дне маленьких кармашков оболочки находились стволовые клетки (на рисунке они темные).
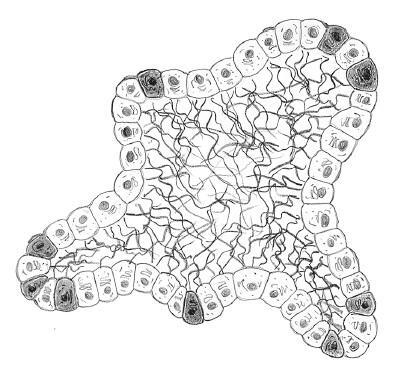
Иными словами, стволовая клетка кишечника создает органоид, похожий по форме и поведению на реальный орган достаточно, чтобы использовать его, например, в испытаниях препаратов для лечения болезней кишечника.
Что касается глаз, Ёсики Сасаи и его коллеги из японского Института физико-химических исследований (RIKEN) вырастили из стволовых клеток, превращающихся в клетки сетчатки, органоиды в форме почти полусферического впячивания, характерного для зарождающегося глазного бокала (задней части глаза)10.
За несколько лет до этого, в 2008 году, та же группа показала, что из стволовых клеток мыши можно вырастить клубки взаимосвязанных нейронов, напоминающие по структуре область коры мышиного мозга11. В 2013 году венская лаборатория Юргена Кноблиха, входящая в состав Австрийской академии наук, вырастила «церебральные органоиды», воссоздающие несколько слоев головного мозга с функциональными нейронами и областями, которые напоминали зарождающиеся структуры вроде префронтальной коры, гиппокампа и других12. Хоть этим органоидам и было далеко до рабочего мозга, им сразу же нашлось применение. Команда Кноблиха пыталась выяснить природу микроцефалии – расстройства развития, приводящего к формированию слишком маленького мозга, – и в качестве основы для органоида использовала стволовые клетки человека с этим диагнозом. По сравнению с аналогами, выращенными из клеток здоровых людей, в этих органоидах один тип стволовых клеток претерпевал меньше делений, что выливалось в общий дефицит клеток. Хотя возможность обретения церебральными органоидами чувств или сознания весьма призрачна, ученые и философы уже прощупывают этическую компоненту таких исследований, включая критерии оценки и трактовки способностей нейронных ассоциаций13.
Кишки, глаза, мозги… Полный список созданных органоидов гораздо длиннее и продолжает расти. Как отмечалось, органоиды служат великолепными инструментами, позволяющими использовать совершенно новые подходы в изучении индивидуального развития, болезней и лекарств, поскольку это подобия реальных органов, не заключенные в живых телах и способные строиться из человеческих клеток. Можно даже помечтать, что технологический прогресс однажды превратит органоиды в полноценные органы, готовые к пересадке человеческим реципиентам.
Органоиды не только приносят практическую пользу, но и дают нам восхитительный биофизический урок. Мы уже не раз упоминали о самосборке – как в молекулярном масштабе, когда белки самопроизвольно укладываются в уникальные формы, так и в организменном, когда по заложенным внутри них принципам строятся целые тела. Сейчас мы видим, можно сказать, модульную самосборку в средних масштабах, возможную благодаря тому, что компоненты разных органов содержат инструкции по собственной организации. Для наглядности можно представить, что не только автомобиль формируется из маленького зачатка, но и обломок двигателя вырастает в полноценный ревущий мотор, если омывается подходящим моторным маслом и закреплен подходящими деталями, а фрагмент водительского сиденья превращается в целое кресло при заботливой поддержке – иными словами, каждый компонент целого в какой-то степени самодостаточен. Природа эксплуатирует самосборку на всех уровнях организации, ступень за ступенью.
Мы помогаем самосборке органоидов, конструируя подходящий внеклеточный матрикс, но после этого пускаем дело на самотек. А что, если бы мы принимали более деятельное и целенаправленное участие в работе самих внеклеточных механизмов? Создание малых объектов, не предназначенных для биологического применения, стало одним из величайших триумфов человеческой цивилизации за последние полвека. Так, наши заводы поразительно быстро и надежно штампуют чипы, ведущие вычисления внутри мобильного телефона, с миллиардами транзисторов, втиснутых в несколько квадратных сантиметров. Наши микропроизводственные возможности гораздо шире набора электродеталей вроде диодов и транзисторов. Применяя пластмассы и гели, например, мы можем мастерить канальцы, стыковочные узлы, клапаны и насосы субмиллиметрового масштаба – как раз то, что нужно для доставки питательных веществ и сигналов группам клеток.
Сочетая микропроизводство с культивированием клеток, мы получаем «органы на чипе», разнообразие которых, как и в случае органоидов, поразительно быстро растет. Несколько из них появились на свет в лаборатории Дональда Ингбера в Институте биологической инженерии Висса при Гарвардском университете. В частности, в 2010 году там создали «легкое на чипе»14. В этой конструкции пористая, мягкая, тончайшая силиконовая мембрана разделяет две камеры, одна из которых наполнена воздухом, а другая – водным раствором, напоминающим кровь. Как мы увидим в главе 11, легкие по своей сути – это место соприкосновения воздуха и воды, где происходит газообмен. По одну сторону мембраны ученые вырастили клетки того типа, который выстилает воздушную сторону легочного интерфейса, а по другую – клетки выстилки кровеносных сосудов. Хитрость же была в том, что торцы мембраны упирались в тонкие стенки камер, приспособленных для закачки и откачки воздуха. Под давлением воздуха стенки сжимали мембрану с наросшими на ней слоями клеток, под вакуумом – растягивали (см. рисунок).